강황 추출물 Curcumin과 신장에 관한 연구
커 h로한long history 그리고has been used as a medicine 을thousands 의years 에서traditional Chinese medicine (리Mengtao etal.2010) 그리고Ayurvedic medicine (Goel et알다.2008). As a traditional Chinese medicine extract, 커has few side 효과at reasonable drug concentrations 그리고has a broad-spectrum therapeutic 효과에diseases. It provides new clinical treatment ideas for malignant tumors, chronic diseases 그리고poor surgical prognoses 에서이cardiovascular, respiratory, nervous, urinary and digestive systems. This paper reviews the latest research progress on the prominent anti-tumor effect 의커and its molecular mechanism 의action on diseases 의different systems.
1. curcumin의 구조와 기능
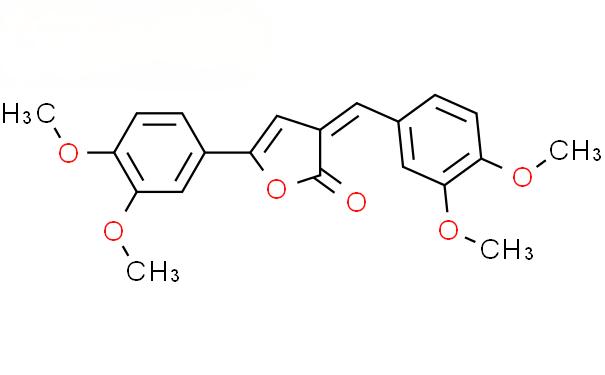
한약재 강황의 리좀은 1~6% 커큐미노이드 화합물을 추출할 수 있다.커큐민은 커큐미노이드 유사체의 60~70%를 차지하며 생물학적으로 가장 활성도가 높은 성분이다.커큐민의 IUPAC 이름은 (1E,6E-)1,7-비스 (4-히드록시-3-메톡시페닐)-1,6-헵타디엔-3,5-디온이며 분자량은 368.38 이고 분자식은 C21H20O6이다.pH 값이 다른 화학환경하에서 커큐민에 7개의 탄소원자가 있는 탄소사슬상의 2개의 케토그룹은 이중 케토-에놀 상호변환을 거칠 수 있기 때문에 인체내의 생리적 pH 조건에서 커큐민의 화학구조는 안정하지 못하다.
이ma에서functions of 커are reflected 에서its functional groups:phenolic groups and diketone structures. These two active functional groups mediate the hydrogen-donating reaction, Michael addition reaction, and a series of hydrolytic and enzymatic reactions of curcumin. 이phenolic hydroxyl group in the structure of curcumin is most likely to undergo a hydrogen-donating reaction, and is then metabolized into a phenoxy group, which exerts antioxidant properties and scavenges reactive oxygen species (ROS), which are composed of molecular oxidants and free radical oxidants. Secondly, curcumin can 행동as a nucleophile and undergo a Michael addition reaction with a strong electrophile, exerting cytotoxic effects on cancer cells, i.e., antitumor 활동(Priyadarsini et알다.2014). In addition, curcumin also has anti-inflammatory, anti-infective, and lipid metabolism-regulating functions.
2. 항종양에서의 curcumin의 분자 기전
오늘날 악성종양은 점점 더 인체건강을 위협하고 있으며 중국의 암 발생률과 사망률도 해마다 상승하고 있다 (우 외 2019년).현재 악성종양의 일반적인 치료법으로는 수술, 방사선치료, 화학요법 등이 있다.그러나 이러한 일반적인 치료 방법은 예후가 나쁘고 재발률이 높습니다.약물 표적 치료 (Seebacher etal.2019)나 면역 치료 (Doroshow et알다.2019)도 점차 약물 내성이 증가하고 부작용이 심해지는 등의 제한점이 있다.
따라서 기존의 악성종양 치료법보다 우수한 방법을 찾는 것이 특히 중요하다.최근 커큐민은 종양세포의 비정상적인 증식, 국소 침입, 전이, 침입을 억제하여 영향을 받은 조직 및 장기의 악성 종양 발생 및 발생을 완화시킬 수 있다는 것이 보고되었다.서로 다른 계통의 악성종양의 병인과 임상양상이 다르거나 완전히 일치하지는 않지만 커큐민은 발생률이 극히 높은 악성종양에 대해 광범위 억제효과가 있다.2018년 통계에 따르면, 진단율 면에서 중국 암 대계의 5대 암은 폐암, 위암, 대장암, 간암, 유방암 (풍외 2019)이다.현재 연구는 커큐민이 우연히이 다섯 가지 암에 중요한 치료 효과가 있다는 것을 보여준다.
커큐민이 폐암에 미치는 영향 및 기전 (1)
폐암은 호흡기 계통의 가장 대표적인 암이다.폐암에는 소세포암과 비소세포암이 있는데,이 중 80% 가 비소세포폐암 (NSCLC)이다 (Evans et알다.2013).의 치료 효과는 커는 여러 메커니즘을 포함 한 폐암의 규정을 비롯 한 Wnt/β-catenin신호 경로, 세포 성장 같은 생활에 관련 한 것이 활동, 세포 사멸, 마이 그레이 션과 차별화;암에서 비정상적으로 발현되는 전사 3 (STAT3) 신호전달 경로의 신호 변환기 및 활성제 (signal transducer and activator;그리고 세포 성장과 같은 생물학적 기전을 조절하는 microRNAs와 nuclear factor eryth-2-related factor 2 (NRF2).STAT3) 신호 경로;micro-RNA (miRNA)와 nuclear factor erythroid 2-related factor 2 (Nrf2)는 세포 성장과 같은 생물학적 기전을 조절하는 신호 경로이다 [1].
임상 인체 폐 조직 샘플에 대한 세포 실험에서는 curcumin이 TLR4/MyD88-EGFR 신호전달 경로를 억제함으로써 NSCLC 세포의 증식과 이동을 현저히 감소시켜 activin-1을 억제하고 상피 중간엽 전이를 억제할 수 있음을 확인하였다 [2].그러나 현재 대부분의 연구는 일부 약제내성 암에 대한 표적치료제와 커큐민의 병용에 초점을 맞추는 경향이 있다.
Chen 등 3명은 gefitinib 내성 NSCLC 세포 실험에서 curcumin과 gefitinib의 결합이 야생형 표피 성장 인자 수용체 (EGFR) 및/또는 KRAS 돌연변이를 가진 NSCLC 환자에서 gefitinib의 효능을 향상시키고 gefitinib 내성을 극복할 수 있음을 발견했다.그 구체적인 기전은 프로테아좀에 의해 유도되는 표피성장인자 수용체 단백질의 분해와 관련이 있을 것이다.Bland 등 [4]은 세포실험을 통하여 curcumin과 그 유도체인 RL66과 RL118이 NSCLC에서 anaplastic lymphoma kinase-positive 폐adenocarcinoma에 억제 효과가 있으며, crizotinib에 대한 교차저항성이 없는 독립적인 표적에 작용한다는 것을 발견하였다.
(2) 위암에 대한 영향 및 기전
다양한 위암 세포주 실험과 일련의 위암 동물 모델 실험을 통해 커큐민 및 그 유사물질들이 항산화 스트레스 및 화학감작 효과를 가지고 있으며, 미토콘드리아 의존적 또는 비의존적 경로에서 여러 신호 경로를 통해 위암세포의 침입, 증식 및 전이를 억제할 수 있음을 확인하였다 (Barati etal.2019).위암세포 (BGC-823)와 마우스 이종 이식 위종양 모델을 이용한 실험 결과, 커큐민 유도체 L6H4가 체외 및 체내에서 위암세포 BGC-823의 증식과 침입을 억제할 수 있음을 발견하였다 (Mu et알다.2019).또한 세포와 생쥐 종양 모델 실험을 이용하여 연구원들은 커큐민 유도체 WZ35에 관련된 연구를 수행하였고 WZ35가 ROS 생성을 유도하고 하마 신호전달 경로의 다운스트림 이펙터 분자인 Yes-associated protein (YAP)을 다운조절하고 c-Jun N-terminal kinase (JNK)를 활성화함으로써 당화를 억제하여 위암세포 증식을 억제하고 세포사멸을 촉진한다는 것을 발견하였다 [5].
최근의 연구 결과에 따르면 커의 조합과 과의 analogues 화학요법의 화학요법 효과에 크게 향상시 킬 수 있는 핵을 활성화 하여 위암으로 요인-κ B (핵 요인, NF-κ B) 및 upregulating 사멸의 수준, 그렇게 함 으로써 upregulating 위암 세포의 민감도를 chemotherapeutic 마약 [6]이다.또한 Kim 등 7은 curcumin이 쥐의 위에서 제1기 대사효소의 발현을 억제함으로써 benzo[a]pyrene-induced DNA첨가 형성을 억제하여 DNA 손상을 억제하여 benzo[a]pyrene-induced 위암 발생을 억제할 수 있다고 보고하였다.
(3) 대장암, 간암, 유방암에 대한 영향 및 기전
가장 대표적인 폐암과 위암 외에도 대장암 (대장암, CRC)의 경우, 인체 대장암 세포주와 CRC 동물모델 실험을 통해 커큐민의 In vivo 및 In vitro 항암 특성을 CRC (Pricci etal.2020;간 세포 암, 간암 (HCC), 세포 실험에서 hypoxia-inducible의 안정성을 억제는 커 있 factor-1 α (HIF-1 α)에 의해 upregulating Nrf2 그리고 글 루타 티 온, 그렇게 함 으로써 유도 ROS 청소, 차례로 결합조직의 표현을 억제하는 성장 인자 (CTGF), 궁극적으로 보호 한 영향을 HCC (샤 오 외다. 2019년);유방암의 경우, 세포 실험 및 이종 이식 마우스 모델 및 폐 전이 모델에서 커큐민 유도체 WZ35는 ROS-YAP-JNK 신호전달 경로를 통해 유방암 세포 성장을 억제할 수 있습니다.(왕외 2019.
3. 다양한 시스템에서 curcumin의 역할
(1) 커큐민은 심혈관계의 보호효과에 참여한다
Atherosclerosis caused 에 의해dyslipidemia and exogenous induced ischemia-reperfusion 부상are common diseases of the cardiovascular system. 커has the effects of lowering blood lipids and resisting oxidative stress, suggesting its potential clinical application value in cardiovascular system diseases. In 셀and mouse experiments, the protective effect of curcumin on cardiomyocytes may be achieved 에 의해downregulating the Notch pathway and 줄이는intracellular ROS levels[8]. In addition, Guan et al.[9] confirmed that curcumin can reduce the decrease in H9C2 cell viability and promote 사멸induced by palmitic 산을 통해activation of the endoplasmic reticulum stress 경로이다.Animal experiments have found that curcumin can also regulate blood pressure. 커can lower blood pressure by 억제angiotensin-converting enzyme and angiotensin II levels in the brain (Kim et 알다.2019).
임상 실험 결과 커큐민은 젊은 비만 남성의 호모시스테인을 낮추고 HDL 농도를 증가시켜 비만 관련 심혈관 질환의 위험 인자를 개선할 수 있는 것으로 나타났다 (Campbell et 알다.2019).또한 커큐민은 경구 복용시 죽상경화증 환자의 LDL 콜레스테롤, 매우 낮은 밀도지단백, 중성지방 수치를 현저히 개선할 수 있다는 임상 실험 결과가 나왔다.이는 curcumin이 지질대사, 지질산화, 산화스트레스 과정에 참여할 수 있다는 사실과 관련이 있을 것이다 (Ding Xiujuan et 알다.2020).관상동맥 미세색전증과 소양증은 경피적 관상동맥 중재술의 흔한 합병증이다.심근 세포 사멸과 염증 반응을 억제는 커 있 TLR4를 억제 함 으로써/MyD88/NF-κ B 신호 경로와 downregulating 염증 성 종양 괴 사 인자의 표현-α (TNF-α)과 interleukin-1 β (IL-1 β), 그리고 궁극적으로 보호 심근 부상 유도 쥐 [10] 관상동맥 microembolism에 묶여 있었다.또한, 쥐의 경동맥 모델을 이용한 실험에서는 커큐민이 신내막 증식을 예방하고 수술 후 혈관 재협착도 억제할 수 있음을 확인하였다 (Akhlaghi et al.2019).
(2) 급성 폐손상에 대한 커큐민 및 그 유사체의 보호효과
급성 폐 손상 (ALI) 및 급성 호흡 곤란 증후군과 같은 호흡기 질환은 종종 염증성 폭풍, 산화 스트레스, 심지어 박테리아 감염을 동반합니다.커큐민은 세 가지 병적 과정을 모두 억제한다.Chai 등 11명은 맹장결찰과 천자로 유도된 생쥐 알리 모델에서 curcumin이 미성숙한 CD4+ T세포의 발달과 CD4+CD25+FOXP3+ Tregs 로의 분화를 조절할 수 있으며, 궁극적으로 대식세포의 변화를 촉진함으로써 항세포사멸, 항염증 및 면역조절 효과를 발휘할 수 있음을 발견하였다.알리의 치료를 위해서는 기존의 커큐민의 경구 또는 복강 내 투여 외에 운반체와 병용하여 약물을 흡입하는 방법도 사용될 수 있다.Kim 등 (12)은 curcumin에 항염증 활성을 갖는 heme oxygenase-1 유전자 플라스미드를 혼합하고, 흡입법을 이용하여이 혼합물을 콜레스테롤과 연관된 poly-amidoamine (PamChol) 운반체를 통해 ALI 생쥐 모델에 투여하였다.이를 통해 기존 투여시보다 우수한 항염증 효과를 얻었다.
게다가, 그레나다 et 알다.[13]에서 발견 되 생체 실험 항 염증 활동에 알리의 평가에 관 한 쥐는 대부분의 합성 dicarbonyl 함유 analogues로 대표 되는 DACs 5a27와 5a28 lipopolysaccharide-induced TNF를 억제 효과적으로 할 수 있-α와 IL-6 수준, mitogen-activated 단백질을 차단 산화효소 (MAPK) 신호 경로, 항 염증을 행사 NF-κ B, 활성화하고 효과 알리에 반대 한다.또한, 세포 및 동물 실험을 통해 [14] curcumin 아날로그C66은 JNK inhibitor SP600125와 결합하여 JNK의 인산화, 즉 MAPK 경로를 억제함으로써 염증성 사이토카인의 발현을 억제하여 궁극적으로 염증 반응을 완화시키고 lipopolysaccharide의 intratracheal instillation에 의해 유발되는 급성 폐 손상을 감소시킬 수 있음을 발견했다.산화 스트레스를 포함한 파라콰트의 섭취에 의한 일련의 독성 효과는 폐 기능을 심각하게 손상시켜 알리로 이어지는 경우가 많습니다.실험결과 curcumin 배양이 paraquat 전처리 정상폐섬유모세포 (WI-38VA13)의 ROS 수준 및 세포자멸사율을 현저히 감소시키는 것으로 밝혀졌으며, 이는 TXNIP/NLRP3 염증축의 억제와 관련이 있을 것으로 보인다 [15].
신경질환에 대한 커큐민의 생물학적 효과 (3)
Curcumin은 우울증 치료를위한 복합 한약의 주요 성분이며 (리Chuanpeng et 알다.2020), 현재 일반적으로이 치료 기전이 시상하부-뇌하수체-부신 축 (HPA 축)의 조절과 관련이 있을 것으로 여겨지고 있습니다, HPA 축) 규정;이는 도파민 및 세로토닌과 같은 모노아민 신경전달물질의 조절 장애 및 뇌유래 신경영양인자 (brain-derived neurotrophic factor;염증과 면역 경로 조절 장애 [16] 와도 관련이 있다.임상시험에 기반한 메타분석에서 연구진은 커큐민을 우울증 보조치료제로 어느 정도 인정해줬다.그러나 이러한 메타분석 역시 시료의 수와 품질에 따라 한계가 있으며, 커큐민의 임상적 효능은 좀 더 평가될 필요가 있다 (Fusar-Poli et 알다.2020).
위와 같은 신경정신질환에 대한 커큐민의 치료효과를 고려하여 현재 임상시험은 높은 치료율 달성을 궁극적인 목표로 하여 커큐민의 신경학적 합병증 완화 효과를 연구하는데 중점을 두고 있다.한 임상시험 결과 8주간의 지속적인 나노커큐민 보충제가 당뇨병성 말초신경병증 환자의 우울 및 불안 점수를 감소시키는데 위약군보다 우수함을 확인했다 (Asadi 등 2019).분자 함유 개입의 메커니즘의이 측면에서 neuroinflammation, 장 et 알다.[17] 첫째는 커 표현을 홍보 할 수 있 다는 것을 발견 했 혁신을 통해 microglia의 TREM2/TLR4/NF-κ B 신호 경로 neuroinflammation을 줄이는 것이다.우울 기분은 통증 역치의 감소를 가져올 수 있고, 커큐민은 우울 장애와 수술 후 통증을 완화시킬 수 있지만, 둘 사이의 관계와 메커니즘은 아직 해명되지 않았다.신경 퇴행성 질환 측면에서 커큐민은 에탄올로 유도된 생체 내 및 생쥐의 체외 실험에서 Nrf-2/TLR4/RAGE 신호전달 경로를 통해 산화 스트레스, 신경 염증 및 세포사멸을 억제하여 신경 퇴화 및 인지 기능 장애를 개선할 수 있다 [18].또한 커큐민은 중금속과 킬레이트하여 쥐의 소뇌에서 납으로 유도되는 산화 스트레스를 억제하여 운동 및 인지 기능 장애와 신경세포 기능을 개선할 수 있다 [19].
(4) Curcumin', s 신장 조직 손상에 대한 완화 효과
Curcumin은 급성 신장 손상의 마우스 모델에서 lipopolysaccharide에 의해 유도된 신장 조직 손상을 현저히 감소시키고 lncRNA PVT1의 발현을 억제할 수 있습니다.게다가,이 결과는 curcumin&와 관련이 있을 수 있습니다#39; s 억제의 PVT1/JNK/NF-κ B 신호 경로 [20].황등 (21)은 curcumin이 miR-81a/PTEN 축을 통해 생쥐에서 시스플라틴으로 유발된 급성 신장 손상의 신독성도 완화할 수 있음을 발견하였다.게다가, 셀과 마우스 모델 실험 함유 패혈증을 줄 일 수 있 다는 것을 확인 했을 억제 하여 급성 신장 부상 NF κ B와 JAK2/STAT3 신호 통로 (2020년 Zhu et al.)이다.또한, lipopolysaccharide-induced RAW264.7세포로 실험한 결과, curcumin은 대식세포에 의해 유도되는 type C lectin을 억제하여 M1대식세포의 표현형을 유지하고 궁극적으로 급성 신장 손상을 감소시킬 수 있음이 밝혀졌다 [22].
커큐민은 만성 신장질환에도 이로운 효과가 있다.함유 할 수 있는 down-regulate 요산 수치에 의해 hyperuricemia 유도의 마우스 모델에 칼륨 oxonate, 더 억제 NLRP3 inflammasome 요산에 의해 활성화와 IL-1 β 수준, 그리고 궁극적으로 인한 만성 신장 염증을 억제 hyperuricemia [23].Li 등 (24)은 glyoxalate에 의해 유도된 신장결석의 실험 생쥐 모델에서 curcumin이 항산화 스트레스, 항염증, 항세포사멸, 항섬유화, 자가포식 기전 억제 등 여러 가지 기전을 통해 카옥스 결정의 침착과 이와 관련된 신장조직의 손상을 효과적으로 감소시킬 수 있음을 발견하였다.CaOx 결정의 침착과 이에 수반되는 신장조직의 손상을 감소시킨다.그러나, 관련 분자 메커니즘에 대한 연구 측면에서, 이번 실험은 커큐민이 Nrf2 신호 경로를 통해 적어도 부분적으로 반석 기능을 발휘한다는 것을 초보적으로 발견했을 뿐이다.
(5) Curcumin', s의 간조직 손상 완화 효과
커큐민이 소화 기관 (간 및 췌장 등)의 병적 및 생리적 손상을 완화시키는 메커니즘은 복잡합니다.고전적 경로는 염증성 사이토카인과 산화 스트레스에 의해 매개되는 면역 경로와 관련이 있다.커의 행정부 결합과 Erzi Wan 염증 성 cytokines의 수준을 억제 할 수 있 (IL-4과 TNF-α) 유도 Concanavalin와 쥐에 한 면역, 형 간염에 의해 그들의 혈청 수준의 alanine downregulate aminotransferase과 aspartate aminotransferase, 그렇게 함 으로써 염증과 병리 학적 간 손상을 완화을 절감 합니다.구체적인 메커니즘은 Nrf-2 신호 경로 [25]의 억제와 관련이 있을 수 있다.
루오et al.[26]은 Nrf-2가 위치한 분자 경로에 대한보다 자세한 연구를 수행하였다.그들은 curcumin의 두 가지 가수분해 대사산물인 tetrahydrocurcumin과 octahydrocurcumin이 CYP2E의 활성과 발현을 억제하고 Kelch-like ECH-associated protein 1 (Kelch-like ECH-associ- ated protein 1, Keap1)-nuclear factor E2-related factor 2 (nu- clear factor-E2-related factor 2, Nrf2) pathway, 생쥐에서 아세트아미노펜으로 유발된 간 손상을 개선한다.커 무 알콜을 완화 할 수도 있 고지 방 식단 지방이 많은 간질환로 인한 쥐 개선 함 으로써 장내 기능, 장벽이 줄이 내 독소, Toll-like receptor-4 (TLR4)와 NF-[27] κ B 염증이 생 긴 것이다.Luo 와는 달리 비알코올성 간청진증의 치료를 위해 Gheibi 등 [28]은 쿠르큐민을 우르소데옥시콜산과 함께 사용했으며, 쥐를 대상으로 한 실험을 통해 쿠르큐민 단독과 유사한 개선 결과를 얻었다.그러나이 병용요법은 curcumin이나 ursodeoxycholic acid 단독요법보다 더 효과적이었다.
4. 결론 및 전망
Curcumin은 여러 분자 경로의 중재를 통해 다양한 인간 시스템 및 기관에 긍정적인 생물학적 효과를 발휘합니다.커큐민은 혈중 지질 수치를 조절하고 산화 스트레스를 억제하며 혈압을 조절해 심근세포와 혈관에 세포 사멸 방지, 염증 억제 등의 보호 효과를 발휘한다.알리로 대표되는 호흡기 질환 치료에서 커큐민과 그 유사체는 항염증 및 산화 방지 스트레스 효과 외에도 면역 조절 역할도 한다.신경질환의 경우 커큐민은 신경 및 정신질환을 완화시키기 위한 보조요법으로 주로 사용된다.
In addition, curcumin also 덜어the corresponding damage to 신장and 간tissues in urinary and digestive system diseases. Therefore, curcumin, which has many pharmacological properties, has good research and application prospects. However, the oral bioavailability of curcumin is relatively low. Therefore, the current research and development of drugs that modify the structure of curcumin, the activity screening of curcumin analogues, derivatives, and 대사 물질with similar functions, and the study of their mechanisms of action are of high research value. Although cell experiments, animal experiments and clinical trials have confirmed that the mechanism of action of curcumin is related to the interaction of multiple pathways, the specific molecular mechanism of curcumin in each signaling pathway has not yet been elucidated in detail. In addition, clinical pharmacokinetic concentration screening experiments with different gradients still need to be carried out for a specific disease in a certain system and for a certain age range of patients in order to determine the safe and effective curcumin use concentration range. This study provides a theoretical basis for the future combination use of curcumin and as a biological health care drug.
Referenece:
[1] 아슈라피자데 M, 나자피 M, 막반디 P, et al. 폐암 thera-py에서 curcumin의 다용도 역할 및 그 유도체. J세포 의술, 2020년, 235 : 9241~9268.
[2] 장 L, 타 오 X, 푸 Q, et al. 커 억제 세포 증식 및 마이 그레이 션 NSCLC에서 을 통해 a TLR4/MyD88and EGFR 경로에 syner-gistic effect. Oncol Rep, 2019, 42: 1843년~1855년.
[3] 첸 P, 황 HP, 왕 Y, et al. 커 오버-come 기본gefitinib 저항 in non-small-cell 폐암 세포 을 통해 유도 autophagy-related 셀 죽음이다. JExp Clin 암 Res, 2019, 38: 254.
[4] 블랜드 AR, 바우어 RL, 니믹 M, 호킨스 BC, 로젠-그렌 RJ, 애쉬 톤 JC다. Cytotoxicity of curcumin deriva-ALK 양성 비소세포 폐암에서 약제. Eur J Pharmacol, 2019, 865 쪽 : 172749.
[5] 첸 T, 자 오 L, 첸 S, et al. The curcumin 유사체 wz35는 ROS-YAP-JNK 경로를 통해 위암세포의 당질 억제에 영향을 미친다. 식품 Chem Toxicol, 2020년, 137 : 111131.
조우 [6] L, Li Y, 그는 W, et al. 상호 적대감 Wilms&의#39; 종양 1and β-catenin 명령 podocyte 건강과 질병. J Am Soc Nephrol은, 2015, 26 쪽 : 677.
[7] 김 KS, 김 뉴욕, 아들아 JY, et 사 al. 커 벤조 [a] 피레네 유도를 개선한다 DNA 손해 in 위 tis-의 고소 sprague-dawley 쥐다. 정수 J Mol Sci, 2019년, 20 : 5533.
[8] 주 P, 양 M, 헤 H, 외.Curcumin은 hypoxi-a/reoxygenation-induced를 약화시킵니다 cardiomyocyte 부상 by down-노치 조절 신호를 보내다. Mol 의대의원, 2019, 20 : 1541~1550.
[9] Guan G, Lei L, Lv Q, et al. 커 흐르면서 pal-mitic acid 유도 cell apoptosis by inhibiting H9C2cardiomyocytes에서 endoplas-mic reticulum stress를 받는 경우. Hum Exp Toxicol, 2019, 38: 655~664.
[10] 류 Y, 류 Y, Huang X, et al. 보호 effects 그리고 관상동맥에 의해 유발된 심근손상에 대한 curcumin의 기전 microembolization다. J 셀 Biochem, 2019년, 120: 5695~5703.
[11] 차이 YS, 첸 YQ, 린 SH, et al. 커큐민은 나이브 CD4+의 분화를 조절한다 T 세포 and IL-10immune 활성 화합 변조 반대 급성 lung 부상 쥐에 있다. 생물 의학Pharmacother, 2020, 125 쪽 : 109946.
[12] 김 G, Piao C, 오제이 (Oh J), 리 M. 결합 배달 curcumin과 heme oxygenase-1의 유전자 사용 니까요-terol-conjugated polyamidoamine for 급성 폐 손상에서 항염증 치료. Phytomedicine, 2019, 56 쪽 : 165~174.
[13]Qian J, 첸 X, 슈 S, et al. 디자인과 합성 (Design and synthesis) curcumin의 no-vel di-carbonyl 유사체 (DACs) act as lps로 유발된 급성 폐 손상 (ALI)에 대한 po-항염증제를 텐트로 친다. Eur J 의대Chem, 2019, 167 : 414~425 쪽.
[14] 샤 오 Z, 수 F, 주 X, et al. 억제 JNK의 인광-rylation by curcumin analog C66 보호 lps로 인한 급성 폐 부상이다. 마약 데스 Devel 더, 2019, 13 : 4161~4171.
[15] 렌이, 양 Z, 태양 Z, et al. 커 relieves 3-mediated를 포함하는 thiore-doxin 상호작용 단백질/NLR pyrin domain을 억제함으로써 pa-raquat에 의한 폐 손상 염증 성 pathway. Mol Med Rep, 2019, 20: 5032~5040.
[16] 장 Y, Li L, 장 J. 커 in 항우울제 치료: 잠재력 (potential)에 대한 개요 메커니즘 임상/임상시험 전 및 진행 중인 과제. 기본 Clin Pharmacol Toxicol, 2020년, 127 : 243~253.
[17] 장 J, 정 샤 오 위 Y, Luo Y, et al. 커 microgli-al M2를 촉진하여 lps로 유발된 신경염증을 억제합니다 양극 화를 을 통해 TREM2/ TLR4/ NF-κ B 경로-BV2cells에서 ways. Mol Immunol, 2019, 116: 29일~37.
[18] Ikram M, 사이드 K, 칸 A, et al. 의 자연식 sup-plementation curcumin 보호 쥐 뇌 ethanol-oxidative stress-mediated neurodegener에 대하여-ation과 메모리 장애 을 통해 분노 가 Nrf2/TLR4/신호다. 영양소를 연변일보 2019, 11 : 108.
[19] 아부 K, Mailafiya 음, Danmaigoro 한, et al. 커 흐르면서 lead-induced cerebellar 독성 쥐 을 통해 chelating activity and 억제 of 산화 스트레스. 생체 분자, 2019, 9일 :453.
[20] 황 W,리 X, 왕 D, et 알다. 커 줄 LPS-유도 패혈제 급성 kidney injury through lncRNA PVT1in 마우스의 억제.생명 Sci, 2020, 254: 117340.
[21] 황 SJ, 황 J, 얀 YB, et al. 에서 시스플라틴 유발 급성 신장 손상에 대한 curcumin의 renoprotective effect 쥐: 개입 of miR-181a/PTEN 축. Ren 실패, 2020년, 42: 350~357.
선 탠 [22] RZ, 류제이 (류J), 장 YY, et al. Curcumin mincle-maintain 억제를 통해 시스플라틴으로 인한 신장 염증을 완화 M1 대식 세포 개체다. phyto-medicine, 2019, 52 : 284~294.
[23] 첸이,리 C, 두안 S, 외.커 흐르면서 포타스-시움 옥소네이트 유발 고요산혈증과 신장 인플람-화 in 쥐다. 생물 의학 Pharmacother, 2019년, 118 : 109195.
[24]리 Y, 장 J, Liu H, et al. Curcumin 생쥐의 glyoxylate-induced calcium oxalate 침착과 renal inj uries를 개선한다. Phytomedicine, 2019, 61 쪽 : 152861.
[25] Li Y, Shao Y, Tang H 등.생쥐의 강낭콩 단백질 a 유도 면역간염에 대한 얼지완과 병용한 커큐민의 보호효과.Shizhen National Medicine 국민의학, 2020, 31:769-773.
[26] 루오 DD, 첸 JF, 류제이 (Liu JJ), et al. Tetrahydrocurcumin과 octahydrocurcumin, the primary and 최종 경화 metabolites of 커, 소유 우수 한 그는-patic-protective effect 반대 아세트아미노펜에 의한 간 손상: cyp2e1 및 Keap1-Nrf2 경로의 역할. Food Chem Toxicol, 2019, 123: 349~362.
[27] 펑 D, 조우제이 (Zou J), Su D, 외. Curcumin은 ApoE-/-마우스에서 고지방 식이로 유발된 간질균을 개선함으로써 예방합니다 장 장벽 함수 and reducing endotoxin과 간 TLR4/NF-κ B 염증이다. Nutr Metab (Lond),2019, 16 : 79.
[28] Gheibi S, Ghaleh HEG, 모틀라흐 BM, et al. therapeu-커큐민의 틱 효과 및 ursodexycholic acid on -이아 닌 알코올 지방이 많은 liver 질병이다. Biomed Pharmacother, 2019, 115: 108938.


 영어
영어 프랑스
프랑스 스페인
스페인 러시아
러시아 한국
한국 일본
일본




