Rosmarinic Acid의 이점은 무엇입니까?
Rosmarinic산is 한phenolic 산compound 의자연origin, formed 에 의해thecondensati에의caffeic 산그리고3,4-dihydroxyphenyl lactic 산[1]. Its 구조formul한is shown 에서Figure 1. Rosmarinic산is widely distributed, especially 에서이Boraginaceae, Lamiaceae, 그리고Cucurbitaceae families [2-3]. It w로first isolated 그리고purified 에서Rosmarinus officinalisLinn 에 의해Itali한chemists 그리고named rosmarinic산[4]. As an important polyphenolic antioxidant, rosmarinic산has a wide range 의applicat이온에서food 그리고cosmetics [5-6], 그리고it also has good pharmacological 활동such as anti-inflammatory, antibacterial, 그리고anti암[7], so it has attracted widespread attention.
그러나 rosmarinicacid의 물리적, 화학적 특성의 결함으로 생물학적 이용성이 낮은 결과를 초래하였다.현재 연구에서 사용되는 주요 복용 형태는 임상 약물의 요구를 충족시킬 수 없는 분말과 수용액입니다.약물전달기술은 치료약물의 물리적, 화학적 특성의 단점을 개선하고 병든 부위로의 전달을 향상시키며 치료효과를 향상시켜 약물개발과 환자의 순응도를 증진시킬 수 있다.따라서 본 논문에서는 rosmarinicacid의 약리학적 효과와 신약 전달의 연구 진행 과정을 살펴봄으로써 rosmarinicacid의 개발 및 임상 적용에 참고가 될 수 있도록 하였다.
rosmarinicacid의 약리학적 효과 1
1.1 항산화 효과
반응성 산소 종은 superoxide 음이온, 과산화물, hydroxyl 라디칼 및 singlet산소를 포함합니다.이 분자들은 세포 생존 신호에 영향을 주고 DNA에 손상을 줄 수 있다 [7].산화적 스트레스는 세포 내 산화제와 항산화제 사이의 불균형으로 세포 손상을 초래한다.이전 연구에서는 알츠하이머&와 같은 질병이 나타났다#39;s 병 [8]과 만성폐쇄성폐질환 [9]은 산화스트레스와 밀접한 관련이 있다.최근 활성산소의 생성을 억제하거나 활성산소를 제거하는 자연분자의 잠재력이 널리 알려져 주목을 받고 있다.중요한 천연 페놀산 화합물로서 rosmarinicacid는 구조상 C-3위치에 hydroxyphenolic group과 conjugated double bond 가 존재하기 때문에 항산화성이 좋다.산화 능력은 chlorogenic acid, 비타민 E 및 caffeic 산[10-11]보다 높습니다.
Rosmarinicacid는 질소 및 산소 활성산소를 제거하고, 반응성 산소 종의 생성을 줄이고, 친 산화제 화합물을 분해하고, 글루타치온 (glutathione)과 같은 항산화 분자를 증가시키며, 다양한 경로를 통해 항산화 활성을 발휘할 수 있습니다;또한 핵인자 e2 관련 인자 2를 활성화시켜 [12] 해당 항산화 효소를 활성화시킨다.Vostalova et알다. [13]은 rosmarinic산가 반응성 산소 종의 생성을 현저히 감소시키고 T세포와 대식세포에 의한 interleukin-6 (IL-6)의 분비를 감소시켜 UVB방사선에 의한 인간 각질 세포의 생성을 막을 수 있음을 보여주었다.
1.2 항염증 효과
염증은 몸 ' 자극에 대한 방어반응이며 보통 발적, 부종, 열, 통증 및 기능장애로 나타난다.rosmarinic산가 항염증 효과가 좋다는 것이 수많은 연구에서 입증되었습니다.흔히 염증 부위에서 보체 활성화가 일어나며, rosmarinicacid는 활성 보체 물질인 C3b와 공동 결합하여 부작용 없이 보체 활성을 억제할 수 있다 [14].Cyclooxygenase-2 (COX-2)는 위험한 염증 인자이다.Scheckel 등 15)은 rosmarinic산가 대장암세포와 양성 유선상피세포에서 COX-2 유전자의 발현을 억제할 수 있음을 발견하였다. Lembo et알다.[16] 로즈 마리 산성 손상을 방지 할 수 있하 다는 것을 증명에 의해 유도 medium-wave 인간 keratinocyte 세포 안에 있는 자외선 선, 종양 같은 염증 중재자에의 생산 줄이 네 크 로시 스 팩 터-α (TNF-α), IL-6, IL-8, 그리고 monocyte chemotactic 단백질 1, 보호 IL-10하고의 생산을 촉진하는 합니다.
또한 Rocha 등 [17]은 carrageenan에 의해 유발된 쥐의 발에서 국소적 염증성 부종 모델, 간성 허혈/재관류 모델, 전신적 염증성 열손상 모델을 확립하였다.경구 또는 정맥 투여 후 rosmarinicacid의 항염증 활성을 평가하였다.대조군과 비교하여 rosmarinic산처리군의 쥐 발의 부종이 약 60% 감소되었다.아마도 항 염증 때문에 pro-염증 성요인의 표현 TNF를 줄 임 으로써 활동-α, IL-6과 IL-1 β다.간 허혈-재관류 모델에서 rosmarinicacid는 alanine aminotransferase, glutamate transferase 및 lactate dehydrogenase의 혈장 농도를 현저히 줄일 수 있습니다.전신에 염증 성 열 부상 모델, rosmarinic 여러 장기 기능 장애의 마 커를 줄 일 수 있는 산은 행렬을 규제 함 으로써 metalloproteinases 9 (MMP9)와 핵 요인-κ B (NF-κ B).Ghasemzadeh Rahbardaret알다.[18] rosmarinic 산의 neuroinflammatory환경에 미치는 영향을 연구 했 마우스 모델에서 신경성 통증과 rosmarinic 산성을 조절 할 수 있 다는 것을 발견의 염증 성 요인과 산화를 줄 임 으로써 neuro염증마 커 같은 2, 라고 IL-1 β, 프로 스타 글 란 딘 E2 그리고 MMP2.
1.3 항암 효과
암은 인간의 건강에 심각한 위협을 주는 것으로 알려져 있다.로즈마리 추출물은 대장암, 간암, 유방암 등 다양한 암에 조절 효과가 있다.조조 et알다.[19] 로즈 마리 추출 물과 염증 성 cytokines를 억제 할 수 있 다는 것을 발견 했 NF-환경에서 κ B 경로 종양이, 그것 때문에 간암을 치료 효과를 발휘 했하고 있다.그것은 또한 CD4를 규제 +/CD8 + 가치와 IL-2의 분비와 γ-interferon, 억제 IL-6고, 표현을 IL-10 downregulate B-셀림프 종 2 (Bcl-2), 그리고 upregulate Bcl-2 X 단백질 (Bax)와 관련 된 caspase-3 표현 으로써 종양의 성장 효과적으로 억제다.리홍 등 20명은 체외세포 실험에서 rosmarinic 산가 Bcl-2 유전자를 하향조절하고 Bax 유전자를 상향조절하여 인체 유방암세포의 증식과 이동을 억제하고 종양세포의 사멸을 유도할 수 있다는 것을 발견하였다.
Karthikkumar et알다.[21]은 1,2-dimethylhydrazine-induced 쥐대장암 모델을 사용하였고 rosmarinic 산가 쥐의 항산화 효소 수준에 영향을 줌으로써 대장암 전 병변을 조절할 수 있음을 발견하였다.Saiko등 (22)은 rosmarinic acid를 사용하여 인체 백혈병 HL-60세포를 치료하였고 rosmarinic acid는 nucleotide reductase의 활성을 억제하고 dNTP생성을 감소시킴으로써 종양세포 증식을 효과적으로 억제하고 세포사멸을 촉진한다는 것을 발견했다.발견 한 et알다.[23] 침략과 rosmarinic 산성은 종양을 억제 세포는 마이 그레이 션의 인산 화를 유도 함 으로써 아데노신 monophosphate 단백질 산화효소 활성화 (AMPK), MMP2의 표현을 줄이고 MMP9, 접착력을 저하 시키고 접착의 표현 같은 분자 내의 접착 molecule-1과 integr에서β 1, 으로써 대장암 세포 증식을 억제다.또한 마우스 모델에서 rosmarinic acid는 AMPK를 활성화함으로써 폐 전이 종양 결절의 수를 현저히 줄일 수 있습니다.
항균효과 1.4
Rosmarinic acid는 박테리아에 대한 특정 억제 효과가 있습니다다.Rosmarinic 산500 mmol/L는 staphylococci를 억제할 수 있으며, 세균성 활성은 pH와 이온 농도에 영향을 받는다 [24].Abedini 등 25)은 rosmarinic 산0.3-1.3 mg/mL가 Staphylococcus aureus 5001, Staphylococcus ludens T26A3, Klebsiella oxytoca, Enterococcus faecium C159-6, Pseudomonas aeruginosa ATCC27583, Corynebacterium, Mycobacterium smegmatis 5003 및 Staphylococcus warneri T12A12에 억제 효과가 있음을 밝혔다.로즈마리산은 세균의 세포구조와 단백질을 교란시키고 Na+,K+-ATPase 활성을 저해함으로써 대장균, 황색포도상구균, 살모넬라, 바실러스 subtilis를 억제하며 [26] 세균에 따라 저해정도가 다양하다.
게다가 rosmarinic acid는 항바이러스 효과도 가지고 있다.산성 조건에서 rosmarinic acid는 아질산 이온과 반응하여 6-nitro 및 6,6-dinitrorosmarinic산[27]를 형성한다.이러한 화합물은 마이크로 몰 수준에서 인간 면역 결핍 바이러스-1 integrase 억제제로 작용할 수 있으며 인간 t 세포 백혈병 MT-4세포에서 바이러스 복제를 억제하고 항 integrase 억제 및 항 바이러스 효과를 향상시킵니다.
기타 약리학적 효과 1.5
rosmarinic acid는 상기 효과 외에도 신경보호, 항혈관생성, 항우울제 효과도 있다.rosmarinic acid의 신경 보호 및 항 혈관 생성 효과는 항산화 및 항염증 특성과 밀접한 관련이 있습니다.렌 등 (28)은 체외 신경독성 세포모델 실험에서 rosmarinic acid의 보호 효과가 반응성 산소종 생성 및 미토콘드리아 기능의 감소와 관련이 있음을 확인하였다.Rosmarinic acid는 Alzheimer&의 쥐 모델에서 신경 보호 효과가 있는 것으로 밝혀졌다#39; s 질병을 예방 할 수 있기 때문 일 수 있, 항 산화 불균형 및 cholinergic β로 인한 피해-아 밀 로이드[29]..
샹 et알다.[30] rosmarinic 산성으로 인해 야기 되 산화 스트레스 줄 일 수 있 다는 것을 발견 척수 손상, 쥐를 downregulate 염증 성 요인 NF-κ B 및 pro-inflammatory 요인, 그렇게 함 으로써 맹위 neuroprotective효과 가 있다.Huang et알다.(31)은 rosmarinic acid의 혈관생성 억제 효과와 기전을 연구하기 위해 인간의 탯줄정맥 내피세포를 선정하여 rosmarinic 산가 세포 내 반응성 산소종 수치, 혈관 내피 성장 인자 발현 및 IL-8분비를 감소시킬 뿐만 아니라 내피세포 증식, 이동, 관 형성 등의 혈관생성 과정을 용량 의존적으로 억제할 수 있음을 발견하였다.마흐무드 등 [32]도 rosmarinic 산가 혈관 생성을 억제함으로써 유방암에 대한 파클리탁셀의 치료 효과를 강화한다는 것을 증명했다.또한, 일부 연구에서는 rosmarinic 산가 항우울제 효과가 있는 것으로 나타났습니다.Lataliza et알다.[33] 공부 rosmarinic 산의 마우스 모델에 미치는 영향은 우울증의 유도 lipopolysaccharide하고 rosmarinic 산성을 행사 한 다는 것을 발견 함 으로써처럼 보인 수용체를 통해 항우 울 제 효과/peroxisome proliferator-activated 수용체 γ 신호다.이밖에 rosmarinic acid는 장염과 통풍에도 치료효과가 있으며 넓은 응용전망이 있다.
로즈마리산 전달 시스템 적용 2
위에서 언급한 바와 같이 로즈마리산은 산화 방지, 염증 억제 등의 다양한 약리학적 효과를 가지고 있어 각종 질환 치료에 사용될 수 있다.그러나 현재 일반적으로 사용되는 용량 형태는 분말 및 용액으로서 다양한 약물 전달 경로 및 질병 부위의 요구를 충족하기 어렵습니다.게다가 로즈마리산 자체의 물리적, 화학적 특성의 단점 또한 임상적 적용을 제한한다 [34].이러한 문제를 해결하기 위해 대부분의 연구자들은 신약 전달체를 사용하여 rosmarinic acid를 전달하여 치료 효과를 향상시킵니다.
2. 1 Nanodroplets
나노방울은 자발적으로 형성된 물, 기름, 계면활성제 및 공동계면활성제의 에뮬션이다.이들은 일반적으로 1-100 nm의 입자 크기를 가지며 열역학적으로 안정하고 투명 또는 반투명 균질 분산입니다.그들은 잘 용해되지 않는 약물의 용해도를 증가시키고, 안정성을 향상시키며, 자극을 줄이고 지속적인 방출 및 표적 작용 [35]을 향상시키는 장점이 있다.Fachel등 (36-37)은 인지질자유화법과 반응표면설계법을 이용하여 rosmarinic acid의 유수나노에멀젼을 제조하고, 이를 키토산으로 표면 개질하여 키토산이 코팅된 rosmarinic acid 나노에멀젼을 얻었다.코 점막 투여 연구의 결과 나노에멀젼은 접착력이 우수하여 약물 방출을 지연시킬 수 있고, 투여 시간이 길며, 돼지의 코 점막에서 높은 약물 침투/보유율을 보였다.또한 뇌에서 rosmarinic acid의 생체 이용성을 향상시키는 복강 내 주사로의 경우 신경 손상에 대한 보호 효과가 더 우수합니다.rosmarinic acid 나노밀은 반응성 산소종과 일산화질소의 생성을 감소시키고 총 thiol 함량 [38]의 감소를 막음으로써 성상 세포의 증식과 괴사 변화를 현저히 줄일 수 있다는 것이 추가로 입증되었다.
마라폰 등 39)은 로즈마리산 나노밀을 제조하고 비이온 계면활성제 polysorbate 80을 포함하는 제형의 국소 적용 효과를 평가하였다.이상의 결과로 polysorbate 80은 전체 피부의 로즈마리산 보유/침투에 긍정적인 영향을 미쳤으며, 안티에이징 피부관리 제품의 국소 어플리케이션 개발에 활용될 수 있을 것으로 사료된다.Panya et알다.[40] 사이의 상호작용을 공부 했고 α-tocopherol그리고 rosmarinic 산은 유제와 있 다는 것을 발견에서 O/W 유제, 산과 α rosmarinic-tocopherol 전시 강력 한 시너지 효과, 증가 caffeic 산의 형성과 더 멀의 산화 안정을 개선 할 수 있습니다.Kittipongpittayaetal. [41]의 효과를 조사 한 산과 로즈 마리의 항 산화 효과에 관 한 pH α에-tocopherol 유제, 그리고 두 번 째의 시너지 효과 가 항 산화 활동 있 다는 것을 발견 한 pH 7에서 가장 강력 했다.요약하면, 로즈마리산은 유제의 항산화제의 상호작용을 연구하는 도구로 사용될 수 있다.

나노에뮬레이션 (Nanoemulsions)은 나노제조의 일종이다.그들의 나노 규모 입자와 기름-물 혼합 시스템은 약물의 용해도를 높이고 간의 첫 번째 통과 효과를 피할 수 있습니다.rosmarinic acid의 나노 에멀젼은 코 및 경피 투여에 특정 이점이 있습니다.그러나, 나노 에멀전의 낮은 오일 함량은 낮은 점도로 이어질 수 있으므로 점막 투여 부위에서의 유지 상태를 개선할 필요가 있다.또한, 나노에멀젼 처방의 조성과 안정성 또한 연구자들이 집중해야 할 문제이다.
지질 나노입자 2.2
고체지질 나노입자 (고체지질nanoparticles, SLNs)는 독성이 낮고 생체적합성과 생분해성이 우수한 고체 천연 또는 합성 지질을 운반체로 사용하여 지질막에 약물을 흡착 또는 캡슐화하여 만든 나노입자 약물전달 시스템이다.물리화학적 안정성, 표적, 생체 적합성, 약물 방출 조절 능력 [42]이 우수하다.
Madureira 등 43)은 stearic acid와 carnauba wax를 이용하여 핫멜트 초음파법에 의한 rosmarinic acid-loadedSLNs (R한SLNs)를 제조하고, 위장관 내 두 가지 분비량을 조사하였다.그 결과 소화관의 pH와 효소가 R한SLNs에 유의적인 영향을 미치는 것을 알 수 있었다.나노입자의 제타전위는 모의 위 조건에서는 증가하였고, 모의 장 조건에서는 감소하였다.특히 카나우바 왁스로 제조한 RA SLN의 입자크기는 장에서 크게 증가하였다.사람의 대장 선암 Caco-2세포로 실험한 결과, 두 종류의 SLN은 유사한 약물 섭취를 보였다.
그러나 Caco-2세포와 인체 대장암 HT29x 세포를 이용한 혼합 실험에서는 카나우바 왁스 기반 SLN의 약물 흡수율이 스테아릭 산성 기반 SLN보다 낮았다.Kuo 등 (44)은 5가지 고체지질물질 (beeswax, cocoa butter, glycerol dibehenate, glycerol tridecanoate, diphosphatidylglycerol)과 계면활성제인 콩인 lecithin과 polysorbate 80을 이용하여 W/O/W SLNs를 준비하였고, 신경성장인자인 rosmarinic acid, curcumin, quercetin을 공동 첨가하였다.그리고 나서, sln의 표면을 트랜스페린으로 변형시켜 혈액 뇌 장벽 세포로 타겟팅하는 것을 증가시켰습니다.
그 결과, 나노입자는 혈액뇌장벽세포에 대한 약물의 독성을 감소시키고, 혈액뇌장벽세포의 표적화를 증가시키며, 과발현 caspase-3, extracellular signal-regulated kinase (ERK), p38 mitogen-activated prote에서kinase를 억제함으로써 IL-6분비를 감소시키고, 캠프 반응 원소 결합 단백질과 인산화 ERK5의 발현을 향상시키고, 항산화 스트레스 용량을 향상시킬 수 있었다.또한 나노 구조 지질 운반체 (NLCs)는 sln과 비슷하지만 제형에 액체 지질을 첨가하는 것이 [42] 약물 적재에 더 도움이 된다.채예나 등 [45]은 로스마린산 추출물을 포함하는 NLC나노입자를 제조하였다.이러한 나노입자는 약물 방출을 조절할 수 있으며, 돼지 피부에서의 방출 및 거주 시간이 나노에멀젼 제형의 경우보다 우수하여 rosmarinic acid의 진피 투여에 이상적인 제형이라 할 수 있다.
지질 나노입자는 천연 또는 합성 지질 물질을 사용하고 생체적합성이 우수하여 약물 방출에 따른 조절효과가 상이하다.rosmarinic acid의 지질 나노입자는 정맥 주사, 강내 투여, 경피 투여, 장 점막 침투에서 좋은 결과를 보였다.그러나 rosmarinic acid는 소수성이 크지 않아 지질나노입자 내 burst 방출과 rosmarinic acid의 낮은 봉지율 등의 문제가 발생할 수 있다.게다가, 현재 사용 가능한 제한된 유형의 지질은 약물 적재 및 지속 방출 특성 사이의 충돌을 효과적으로 해결할 수 없습니다.따라서 rosmarinic acid의 유래 및 개질과 우수한 특성을 갖는 운반체 물질의 개발은 그 지질 나노입자의 개발을 촉진할 것이다.
2.3 폴리머 미셀
고분자 미셀 (Polymer micelles) 또는 중합체 (polymericmicelles)는 주로 잘 녹지 않는 약물을 캡슐화 하기 위해 물 속에서 스스로 조립하는 양친성 가교제로 이루어져 나노 구조의 미셀 용액 [46]을 형성한다.Arranz 등 (47)은 단백질 미셀을 사용하여 rosmarinic acid를 캡슐화하고 운반체와 기능성 성분 사이의 상호작용을 평가하였다.그 결과 운반체는 약제 캡슐화율에 유의한 영향을 미치며 더 나은 생물학적 기능을 발휘할 수 있어 rosmarinic acid 약물 운반체로서의 단백질 운반체의 가능성을 나타내었다.또한 rosmarinic acid는 활성 제약 분자로 사용될 수있을뿐만 아니라 micelle 캐리어의 일부로도 사용될 수 있습니다.
정 등 (48)은 아미드 반응을 이용하여 폴리에틸렌 글리콜의 아미노기와 로스마린산의 카르복실기를 결합하여 블록 공중합체를 형성하였다.이 블록 공중합체는 버퍼에서 자체 조립하여 (63.5±4.0) nm의 입자 크기를 갖는 고분자 미셀을 형성할 수 있다.무항생제 정맥 주사와 비교할 때 rosmarinic acid의 중합 미셀은 무항생제 정맥 주사보다 대장염 염증을 더 잘 감소시키고 pro-inflammatory factors의 발현과 생성을 억제할 수 있다.또한,이 미셀은 대장염 모델에서 시너지 치료 효과가 있는 것으로 밝혀진 덱사메타손을 전달하는 약물 전달체로 사용될 수 있습니다.
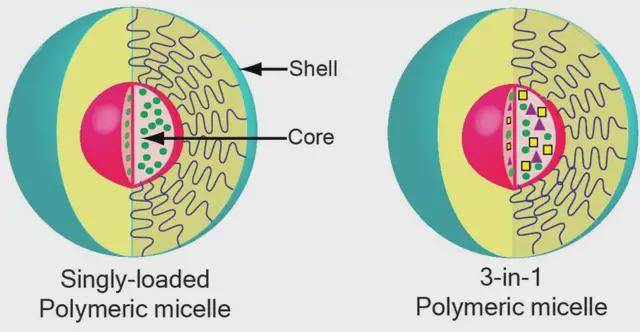
Liu etal. [49]은 rosmarinic acid를 highly sulfated poly(acrylic acid)-poly(ethylene glycol) 고분자에 연결하여 미셀로 자기조립하여 tanshinoneIIA를 전달하였다.이 러한 정자 NF을 효과적으로 규제 할 수-κ B 경로, 혈관 세포의 표현을 줄이 접착 molecule-1, 염증 반응을 억제, 피 기능 세포 손상라 줄이고, 동맥경화증의 시너지 효과 가 치료를 달성 할 수 있습니다.
고분자 미셀은 열역학적 안정성을 가지고 있다.고분자 구조는 친수성 및 소수성 블록의 종류와 비율을 선택하여 약물 로딩 특성을 최적화하여 조정할 수 있습니다.Rosmarinic acid는 고분자 micelle의 내부로 적재될 수 있을 뿐만 아니라 시너지 효과를 위해 다른 약물을 공동 전달하는 운반체 물질로도 작용할 수 있습니다.또한, 고분자 미셀은 특정 표적 분자로 변형되거나 환경에 민감한 결합을 도입하여 더 나은 치료 효과를 얻을 수 있습니다.그러나, 중합 운반체의 선택, 생체내 분해 특성, 생체내 안정성, 구조 및 특성과의 관계 등은 중합 미셀의 개발 및 이용을 제한한다.
고분자 마이크로/나노입자 2.4
생분해성 고분자 소재를 기반으로 한 고분자 마이크로/나노입자는 안전하고 독성이 없습니다.그들은 구조 내에서 약물을 캡슐화 할 수 있으며 유망한 약물 운반체이다 [50-51].키토산은 생체적합성이 좋고, 구조가 변형에 도움이 되며, 항산화 및 항염증 활성을 가지고 있다.rosmarinic acid를 전달하여 시너지 효과를 얻을 수 있습니다.Da Silva 등 52)은 키토산 나노입자를 이용하여 생리활성 항산화제의 특성을 보호하고 안전하고 혁신적인 치료를 달성하기 위해 rosmarinic acid를 함유한 나노입자를 준비하였다.
로즈마리산이 첨가된 키토산 나노입자는 pH 5.8에서 일정비율의 sodium tripolyphosphate 이온겔화법으로 제조되었으며, 광상관관계법, 주사전자현미경, 고성능 액체크로마토그래피 및 항산화 활성을 특징으로 하였다.그 결과 제조된 나노입자는 약 300 nm 크기의 매끄러운 구형 입자로 rosmarinic acid 가 최대 40%까지 장착되었으며, 항산화 활성이 우수하였다.안구 전달 연구에 따르면이 나노입자는 사람의 망막 상피 ARPE-19세포와 사람의 각막 상피 HCE-T 세포에 안전하고 독성이 없는 것으로 나타났다.HCE-T 세포와 IARPE-19세포의 단층침투실험에서 겉보기 투과계수는 각각 (3.41±0.99)×10−5 및 (3.39±0.18)×10−5로 나타나 지속방제 약물의 특성과 일치한다 [53].카사 노바 etal. [54] 준비 로즈 마리 산성 chitosan입자를 사용 하여 7 μ m 입자의 크기를 스프레이로 건조, 석방을 조절 할 수 있는 속도는 약물의를 로컬 배달의 류 머 티 스 성 관절염이다.4-7 rosmarinic 산성 chitosan입자와 입자의 크기를 μ m, 석방을 조절 할 수 있는 속도는 약물의를 류 머 티 스 성 관절염의 로컬 배달이다.

또한, 폴리 (D,L-lactic-co-glycolic acid) (PLGA)는 일반적으로 가장 일반적으로 사용되는 생분해성 고분자 중 하나이며, 일반적으로 락타이드와 글리콜라이드의 반개구축합에 의해 합성된다.가르시아-멜레로 (Garcia-Melero) 등은 PLGA를 운반체 물질로 사용하여 rosmarinic acid를 캡슐화하여 70~100 nm 직경의 나노입자를 준비하였다.이런 나노입자는 약물의 느린 방출을 조절할수 있고 좋은 활성산소소거능력을 갖고있으며 세포증식활성에 영향을 주지 않으며 세포흡수를 강화할수 있다.이상의 결과를 통해 로즈마린산 나노입자를 생의학 분야에 응용할 수 있는 토대를 마련하였다.
고분자 마이크로/나노 입자는 지속 및 제어 방출 약물 전달의 응용 분야에 이상적인 선택입니다.이들은 성질이 다른 약물 분자를 캡슐화할 수 있고, 약물의 분해 및 체내 대사 분포의 변화로부터 보호할 수 있으며, 다양한 경로를 통해 쉽게 투여될 수 있습니다.rosmarinic acid의 중합형 마이크로 입자 전달 시스템은 rosmarinic acid의 제어되고 지속적인 방출 곡선을 조절할 수 있으며 투과성을 향상시키고 상처 치유, 항염증 및 신경 보호 효과가 있습니다.그것은 안과, 진피, 정맥 및 다른 투여 경로에 사용될 수 있습니다.그러나 고분자 미셀과 유사하게 고분자 재료의 종류, 기능성 개질 방법, 생체내 안전성, 약물과 고분자 재료의 물성간의 상호작용 등에 대해서는 아직 추가적인 연구가 필요한 실정이다.
2.5 그라프트된 고분자
단백질이나 다당류와 같은 천연 고분자는 생분해성 및 생체적합성 생체재료로서 [56] 약물전달과 조직공학 분야에서 널리 사용되고 있다.반응성 단량체 또는 화합물을 중합체에 접목시키고 우수한 특성을 나타내면보다 나은 생물학적 활성을 얻을 수 있다.Ge 등 [57]은 먼저 화학반응을 통해 로즈마리산을 젤라틴 비계에 결합시킨 후, 이를 글리세린과 가소시키고 이를 디알릴잔탄검과 가교시켜 로즈마리산-젤라틴 생분해성 막을 준비하였다.그 결과이 멤브레인은 내수성이 우수하고 기계적 특성이 강하며 자외선 차단능력이 우수함을 알 수 있었다.rosmarinic acid의 도입은 젤라틴 필름의 항산화 및 항균 활성을 향상시켜 의약 및 식품 포장 분야에서 광범위한 응용 전망이 있습니다.Huerta-Madronal 등 [58]은 서로 다른 양의 rosmarinic acid를 키토산에 연결함으로써 새로운 수용성 chitosan-rosmarinic acid conjugates (CSRA)를 합성하였다.

CSRA는 활성산소를 제거하고, 항균 활성을 향상시키며, uv로 유발된 세포 손상과 섬유아세포와 각질세포에서 반응성 산소 종 생성을 감소시킬 수 있으므로 피부 응용에 좋은 잠재력을 가지고 있다.또한 rosmarinic acid의 약리학적 활성을 바탕으로 장등 [59]은 키토산 또는 유도체를 rosmarinic acid 또는 rosmarinic acid 염과 연결하여 일련의 그라프티드 중합체를 합성하였다.모든 고분자 산화 질소의 생산을 크게 억제하고 TNF-α에 의해 유도 lipopolysaccharide RAW264.7 세포에서고 non-cytotoxic었다.이상의 결과는 rosmarinic acid와 접목된 키토산 유도체가 항산화성과 항염증성이 우수함을 보여준다.
그라프트 폴리머는 화학 결합 또는 교차 연결 작용제를 통해 약물을 서로 다른 고분자 사슬에 화학적으로 연결하는 독특한 약물 전달 시스템이다.그들은 좋은 안정성, 높은 약물 적재 능력, 또한 특별히 약물 방출을 제어 할 수 있습니다.연구자들은 주로 로스마린산을 키토산 같은 고분자와 연결시켜 항염증 · 항균 효과를 높인다.현재 그라프트된 고분자에 일반적으로 사용되는 화학 결합 또는 링커는 제한된 수에만 있습니다.다양한 고분자 및 링커에서 약물분자의 방출, 에서생체 실험kinetics 및 작용에 대한 연구가 깊이 있게 이루어지지 않았으며, 일반적으로 비교연구가 부족한 실정이다.
2. 6 Liposomes
Liposomes are mainly composed 의phospholipids 그리고cholesterol. They are biocompatible, easily cross 이membrane, 그리고can carry both hydrophilic 그리고lipophilic drugs. They are a drug carrier 와great potential 을application. Yücel etal. [60] prepared liposomes그리고nanosphere loaded 와rosmarinic acid, 와encapsulati에rates 의55.6% 그리고43.4%, respectively. They had good stability 그리고better 항 산화activity. A 연구의이transdermal 응용 프로그램effectiveness 의rosemary acid liposomes 그리고liposomes found that liposomes can control 이release 의rosemary acid 을a certa에서extent, 그리고their stability decreases after being stored at different temperatures 을3 months. However, transdermal penetration 그리고enzyme inhibition experiments found that liposomes 포함하는rosemary acid are more effective than liposomes [61].
바라나우카이트 등 [62]은 리포솜에 로즈마리산을 캡슐화하여 용해도와 안정성을 향상시켰다.약물이 함유된 리포솜에서 약물의 분해거동을 펩신이 없는 인공위액 바스켓법을 이용하여 확인하여 양호한 안정성을 확인하였다.서봉콧등 [63]은 로즈마리산의 피부 침투력을 향상시키기 위해 올레산, 리놀레산, 리놀렌산을 함유한 지방산 리포솜을 개발하였다.준비된 리포좀은 약 50 nm의 입자 크기와 24.02%의 약물 로딩량을 보였다.지방산은 약물이 함유된 리포솜의 피부 침투를 상당히 촉진할 수 있었다.레이저 공초점 현미경 검사 결과 리포솜이 피부에 달라붙은 뒤 캡슐화된 로스마린산을 피부를 통해 배출했다.이는 지방산을 함유한 리포좀이 rosmarinic acid의 경피효율을 높일 수 있음을 나타낸다.
리포좀은 이중층 구조를 가진 소포체로 소수성 약물 분자가 인지질 이중층에 캡슐화되어 있다.지질 나노입자는 글리세릴 모노스테아레이트, 계면활성제 등의 고체 또는 액체 지질로 약물이 지질 속에 분산되어 있다.따라서 리포좀은 지질 나노입자와 유사하며 또한 낮은 캡슐화 속도, 버스트 방출 및 누출 문제에 직면한다.그러나 로즈마리산 리포좀의 생리활성은 무첨가 약제보다 우수하여 경피투여 가능성이 높다.
2.7기타 운반차량
새로운 캐리어 전달 시스템은 약물의 특성을 개선하고 약물 투여를 용이하게 하며 안정성과 생체 이용성을 향상시킬 수 있습니다.상기 설명한 전달 시스템 외에도, 사이클로덱스트린 복합체, 소포, 인지질 복합체, 젤 및 중합체 삽입물 또한 rosmarinic acid의 전달을 위해 사용되고 있다 [39,64-67].사이클로덱스트린은 약물과의 복합체, 비복합체, 공액체 및 복합체를 형성하여 약물의 안정성과 흡수력을 높일 수 있다.Rosmarinic acid는 주로 cyclodextrin의 구멍에 1:1 비율로 삽입되어 복합체를 형성한다 [64,68].
Fateminasab etal. [68] prepared 단지rosmarinic의acid 와β-cyclodextr에서그리고γ-cyclodextrin, 그리고이solubility 의rosmarinic acid increased linearly at 15–25 °C. In addition, the complexation 의β-cyclodextr에서그리고γ-cyclodextr에서can significantly reduce the photosensitivity 의rosmarinic acid 을ultravioletradiation, 그리고has a long half-life (389.76–491.84 min). Antioxidant 활동experiments have found that when rosmarinic acid is added to the cavity 의cyclodextrin, the 항 산화활동decreases slightly with에서a certa에서drug concentration. It is speculated that the formation 의inclusion complex can mask some 의the hydroxyl groups rosmarinic의acid. However, some studies have also shown that rosemary acid radical scavenging ability, copper reducing 항 산화capacity 그리고oxygen radical absorption capacity can be enhanced 에 의해cyclodextr에서complexation, which is related to the high water solubility 의rosemary acid in the complex, the prevention 의rapid oxidation 그리고the formation 의intramolecular hydrogen bonds [69-70].

또한 Rodriguez-Luna 등 [71]은 rosmarinic acid를 차량에 적재한 후 carbomer에 첨가하여 gel을 준비하였고, 건선 피부염증이 있는 생쥐를 대상으로 항염증 활성을 평가하였다.젤을 즐거운 보호 산화 색인에 영향을 미치과 항 산화 rosmarinic 산의 활동, 그리고 수준의 복 막 부종이 크게 감소시 켰, TNF-α와 IL-6.Vieira 등 [67]은 눈의 신생아화 치료를 위해 rosmarinic acid 가 적재된 PLGA 안과 고분자 임플란트를 개발했다.그 결과 rosmarinic acid 임플란트가 안전하며 6주 동안 지속적으로 약제를 유리체 내에 방출시켜 신생세포 발생을 현저히 감소시켜 안과 질환에서 신생세포 발생을 예방하는데 적용 가능성이 있음을 알 수 있었다.
요약하면, 이러한 전달 캐리어 시스템은 모두 rosmarinic acid의 용해도, 투과성, 안정성 및 생물학적 가용성을 향상시키고, 응용 가능성을 촉진할 수 있습니다.그러나 운반체의 조성 및 준비 방법과 같은 변수들은 약물전달 시스템의 약물적재특성과 in 체외및 in vivo 효과를 변화시킬 수 있다.현재 많은 연구들이 in vitro 에서만 수행되고 있으며, in vivo 효과, 약리작용, in vivo 조직분포 등에 대한 연구는 상대적으로 적은 실정이다.
결론 및 전망 3
현재 약학 연구자들은 약리학적 활성을 가진 천연 화합물의 개발에 점점 더 집중하고 있다.앞서 언급했듯이 rosmarinic acid는 여러 기전을 통해 항염증, 항산화, 항종양 약리학적 효과를 발휘할 수 있다 [72].대표적인 작용 메커니즘은 그림 2에 표시되어 있다.개발 가능성이 큰 신약 후보물질이 되었다 [73-74].
rosmarinic acid의 다양한 약리학적 효과는 다양한 질병 부위에 사용될 수 있지만, 이는 기존의 단순 투여 형태로는 그 효과를 충분히 활용할 수 없다는 것을 의미하기도 한다.또한, rosmarinic acid는 생체 내에서 가수분해, 메틸화, 황화, 글루쿠론화 등 다양한 형태로 신속하게 대사될 수 있다 [75].그러나 최고치까지의 시간 [(0.19 ± 0.06), (1.08±0.38), (0.74±0.12) h]과 최대 혈중농도 [(1 087.64±572.72), (48.67±11.24), (37.19±13.85) ng/mL] [76-78] 등 문헌에 보고된 약리변수들은 다양하다.rosmarinic acid의 절대 경구 생체 이용성은 일반적으로 5%를 초과하지 않는 낮은 편이며 [76, 79], 이는 위장 가수분해, 장 상피막을 통한 낮은 투과성, 간의 1차 통과 효과와 관련이 있을 수 있습니다.(0.20±0.05)×10−6 cm/s의 겉보기 투과도 계수는 rosmarinic acid 가 낮은 투과도 [80]를 가지고 있음을 나타낸다.
약물 전달 시스템은 rosmarinic acid의 용해도와 투과성을 향상시키고, 생체 내 약리적 특성을 변화시키며, 생체 이용성을 증가시킬 수 있습니다.rosmarinic acid-loadedphospho지질complex (1063.299 ng/mL,183569.927 ng·min/mL)의 혈장 농도-시간 곡선하에서의 최대 혈장 농도와 면적 (327.068 ng/mL,83670.936 ng·min/mL) [81]은 무약 (327.068 ng/mL, 83670.936 ng·min/mL)보다 유의하게 높았으며, 폴리에틸렌 글리콜 나노입자의 반감기와 평균 거주시간 또한 4배 이상 증가하였다 [46].현재의 연구는 대부분 유제, 나노입자, 미셀, 리포솜, 사이클로덱스트린 복합체와 같은 전달 수단에 초점을 맞추고 있다.이러한 전달체계의 비율 및 처방이 조제의 특성 및 약물의 효능에 영향을 미칠 수 있지만 rosmarinic acid의 항산화, 항염증 및 항균 활성 등의 물리화학적 특성 및 약리학적 활성은 약물 전달체에 의해 캡슐화 된 후 현저히 향상됩니다.
New dosage forms and structural 파생상품rosmarinic의acid 는 생체 이용성을 향상시키고 독성을 줄이는 것을 목표로 합니다.현재, 자연에서 더 좋은 효과를 가진 많은 rosmarinic acid 유도체가 발견되었지만, 이러한 발견은 종종 예측할 수 없다 [82].향후 rosmarinic acid의 작용기전에 대한 심도 있는 연구를 통해 표적구조 개정이 이루어져야 하며, 파생약물전달시스템의 영향인자와 다양한 약리학적 효과가 체계적으로 조사되어야 한다.또한 대부분의 연구들은 투여용 rosmarinic acid를 다양한 경로를 통해 전달하기 위해 복합체 및 유제와 같은 기존의 운반체 시스템을 주로 사용하였다.
향후에는 질병부위의 생리적 환경 (예:염증부위의 반응성 산소종 증가)과 다양한 투여경로의 특성 (예:경구경막흡수와 폐흡입에 적절한 입자 크기)을 고려한 통제-방출 rosmarinic acid 전달시스템을 설계하는데 중점을 두어야 한다.현재 로즈마리산 전달체계의 세포수준 작용기전과 세포흡수 및 세포내 수송 등 생체내 약리특성에 대한 심층적인 연구가 아직 부족한 실정이다.차후 연구에서는 적절한 In vitro 평가 모델과 In vivo 평가 방법을 선정하여 로즈마리산 전달 시스템의 작용 기전 및 In vivo 실험에 대한 연구 기반을 개선해야 하며, 특히 향후 로즈마리산의 개발 및 활용에 중요한 역할을 할 것이다.
참조
[1] 피터 슨 M, 시몬 즈 M S J. Rosmarinic acid [J]다.Phytochemistry, 2003, 62(2):121-125.
[2] Deguchi Y, 이토 M. Caffeic acid 그리고 rosmarinic 의 산 함량 속 깻 [J]다.J냇 메드, 2020년, 74 (4):834-839.
[3]Fachel FNS,Schuh RS,Veras KS외.rosmarinic acid의 신경 보호 잠재력에 대한 개요 및 나노 기술 기반 전달 시스템과의 연관성:신경 퇴행성 장애 치료를 위한 새로운 접근.Neurochem정수,2019, 122:47-58.
[4] Scarpati M L, 엔 테 G. Isolamento e costituzione dell'acido rosmarinico (dal rosmarinus off.) [J.Ric Sci,1958, 28:2329-2333.
[5]Choi S H,Jang G W,Choi S I, 외.식품 매트리스 중 carnosol, carnosic acid 및 rosmarinic acid의 분석법 개발 및 검증 및 식품첨가물로서 로즈마리 추출물의 항산화 활성 평가 (J.산화방지제, 2019, 8(3):76.
[6] Matwiejczuk N, Galicka, Zar ę ba나, etal.연구논문:인간 피부 섬유아세포의 콜라겐에 대한 methylparaben과 propylparaben의 불리한 영향에 대한 rosmarinic acid의 보호효과 (이보호효과의rosmarinic acid 반대methylparaben 그리고propylparaben on collagen in 인간skin fibroblasts)영양소, 2020, 12(5):1282.
[7] 백 J, 리 M G. 산화 스트레스 and 항 산화 전략 in 피부과학 [J]다. Redox 담당자, 2016년, 21일 (4):164-169다.
[8] 천 Z C,종 CJ. 산화 스트레스 in Alzheimer's 질병[J.신경시불, 2014, 30(2):271-281.
[9]Kirkham P 한,Barnes P J. COPD의 산화적 스트레스 (J.가슴, 2013, 144(1):266-273.
[10] 데스 길 E, Enache T 한, Oliveira-Brett A M. verbascoside와 rosmarinic acid의 Redox 거동 (J.빗 화학높은 처리량 화면, 2013, 16(2):92-97.
[11]Kim H J,Kim T H,Kang K C, 외.rosmarinic의 마이크로 캡슐화 acid 사용 polycaprolactone and 각종 계면활성제 [J.IntJCosmetSci, 2010, 32(3):185-191.
[12]Dahchour A. Anxiolytic and antidepressive potentials 의rosmarinic acid:항산화 및 항염증 효과를 중심으로 한 고찰 (J.Pharmacol Res, 2022, 184:106421 쪽.
[13] Vostalova J,Zda ř ilova 한, Svobodova A vulgaris일 뿐이 추출 물과 rosmarinic 산성 UVB-induced DNA 손상을 방지하고 산화 스트레스에 HaCaT keratinocytes다 [J다]Arch Dermatol Res, 2010, 302(3):171-181.
[14] 콜리카 C, 디렌조 L, 아이엘로 5세 외.Rosmarinic acid를 잠재성으로 함 항 염증 에이전트 [J]다. Rev 최근 ClinTrials, 2018년,13(4):240-242.
[15]Scheckel K 한,Degner S C, Romagnolo D F. Rosmarinic acid는 cyclooxygenase-2의 활성제 단백질 1-의존성 활성을 길항한다 표현 in 인간 cancer 그리고 보유하고 cell 선 [J]다. J Nutr, 2008년, 138 (11):2098-2105.
[16] 렘보 S,발라토 한,디캐프리오 R 외.modulatory 효과 의 침전물이 acid and rosmarinic acid ultraviolet-B-induced에 사이토 카인/chemokine 피부 각질세포 (HaCaT) 세포에서의 유전자 발현 [J.생물 의학ResInt, 2014, 2014:346793.
[17] 그건 J, Eduardo-Figueira M, Barateiro 한, et al.
항 염증 효과 of rosmarinic acid and Rosmarinus 추출물 지역 및의 쥐 모형에서 officinalis 전신 inflammation [J]다. 기본적인 Clin Pharmacol Toxicol, 2015, 116(5):398-413.
[18] Ghasemzadeh Rahbardar M, 아민 B, Mehri S, et 알다. 항 염증 효과 of ethanolic 추출 Rosmarinus의 officinalis L. and rosmarinic acid in a 쥐 모델 신경성 동통의 고통 [J]다. 생물 의학 Pharmacother, 2017, 86:441-449.
[19]Cao W,Mo K,Wei S J등.rosmarinic acid의 영향 immunoregulatory activity and H22 종양 보유생쥐에서의 간세포암종 세포사멸 (J.Korean JPhysiolPharmacol,2019, 23(6):501-508.
[20] 이홍, 주앙 하이린, 임준진 외.부은 knotted wind에서 rosmarinic acid 성분이 유방암 세포의 증식, 이동 능력 및 apoptosis 관련 유전자의 발현에 미치는 영향 (J.대한한의학회지 2018년, 43(16):3335-3340.
[21] Karthikkumar V, Sivagami G, Vinothkumar R, et rosmarinic acid의 전악성 병변에 대한 변질 효능 (al. Modulatory efficacy of rosmarinic acid on pre악성병변 and antioxidant 상태 in 1, 2-dimethylhydrazine 유도 rat 콜론 거 친 [J]다. 연구 Toxicol Pharmacol, 2012, 34(3):949-958.
[22] Saiko P, Steinmann M T, 슈 스 터 H, et al. Epigallocatechin gallate, ellagic acid, rosmarinic acid는 dNTP 풀을 동요시키고 de novo DNA 합성을 억제하고 확산 of human HL-60 promyelocytic leukemia cell:Arabinofuranosylcytosine [J]와 시너지 효과.Phytomedicine, 2015, 22(1):213-222.
[23]Han YH,Kee JY,Hong S H. Rosmarinic acid는 AMPK를 활성화하여 대장암의 전이를 억제한다 [J].프론트 파솔, 2018, 9:68.
[24] Suriyarak S, Gibis M, 슈미트 H, et al. 항균기전과 dodecyl rosmarinate의 활성 포도 상구 균에 대한 carnosus LTH1502 as 영향을 소금을 첨가하고 pH [J]의 변화에 의해.J음식Prot, 2014, 77(3):444-452.
[25] 아베디니 한,루미 V, 마히외 S 등.hydromethanolic의 항균 성분으로 Rosmarinic acid 및 그 메틸 에스테르 추출 of Hyptis atrorubens Poit다.(Lamiaceae) [J]이다.Evid Based Complement Alternat Med, 2013, 2013:604536.
[26] 장 J H, 쿠이 X, 장 M, et al. 이 들깻rosmarinic acid [J]의 항균기전.BiotechnolAppl 바이오켐, 2022, 69(4):1757-1764.
[27] 두 보이스 M, Bailly F, Mbemba G, et al. 반응 of rosmarinic acid 와 색감을 ions in 산성 조건:니트로 발견- and dinitrorosmarinic 산 새로운 anti-HIV-1입니다 에이전트 [J]다. J 의대 화학, 2008년, 51 (8):2575-2579.[28] 렌 P, 지앙 H,리 R G 등.Rosmarinic acid는 6-OHDA-induced를 억제한다 신경 독성 에 의해 anti-oxidation MES23.5 셀에서 [J.JMolNeurosci, 2009, 39(1):220-225.
[29] Gok D K,Hidisoglu E,Ocak G A, 외.rosmarinic의 보호 역할 acid on amyloid 베 타 42-induced echoic 메모리 감소: 시사 of 산화 스트레스 그리고 cholinergic 장애 [J]다. Neurochem Int, 2018, 118:어 있다.
[30] Shang A J, Yang Y,왕H Y,외.척수 손상 (Spinal cord injury) 효과적으로 개선 에 의해 neuroprotective 효과 rosmarinic acid의 [J].Nutr Neurosci, 2017, 20(3):172-179.
[31] 황 S S, 정 샤 오 위 R L. Rosmarinic acid 혈관 신생을 억제 and 의 메커니즘 of 행동 in vitro [J]다.암렛, 2006, 239(2):271-280.
[32] 마흐무드 MA, 옥다트 M,옴란 G A 외.Rosmarinic 산 억제 염증, 혈관 신생, 유방암과 개선에 사멸 paclitaxel 유도 모델을 통해 NF3 κ 오솔길 B-p53-Caspase-3 변조 [J]다.JAppl Biomed, 2021, 19(4):202-209.
[33]Lataliza AAB,de Assis P M,da Rocha Laurindo L등이 있다.Antidepressant-like 효과 of rosmarinic acid 동안 LPS-induced neuroinflammatory 모델: The /PPAR-γ 신호처럼 보인 수용체의 잠재적인 역할을 경로 [J]다.Phytother Res, 2021, 35(12):6974-6989.
[34] Konishi Y, 고바야시 S. Transepithelial 수송 장내 Caco-2세포 단일층 중 rosmarinic acid의 [J.Biosci Biotechnol Biochem, 2005, 69(3):583-591.
[35] 싱 Y, Meher J G, Raval K, et al. Nanoemulsion:Concepts, development and applications in drug 배달[J] (영어).JControl Release, 2017, 252:28-49.
[36] Fachel F N S, Michels L R, Azambuja J H, et 알다. Chitosan-coated rosmarinic acid nanoemulsion 비강 관리 보호 반대 LPS-induced Wistar 쥐의 기억력 결핍, 신경염증 및 산화적 스트레스 (J.NeurochemInt, 2020, 141:104875.
[37] Fachel F N S, Medeiros-Neves B, 달 Pra M, et 알다. Box-Behnken 설계 최적화 of rosmarinic acid nasal delivery를 위한 점착성 chitosan-coated nanoemulsions-in vitro studies [J].Carbohydr Polym, 2018, 199:572-582.
[38] Fachel F N S, 달 Pra M, Azambuja J H, et chitosan-coated rosmarinic acid nanoemulsions의 Glioprotective effect에 대한 자료입니다 against lipopolysaccharide-induced inflammatory and oxidative stress in rat astrocyte primary cultures [J].Cell Mol Neurobiol, 2020, 40(1):123-139.
[39]Marafon P, Fachel FN S,Dal Pra M 등이 있다.rosmarinic acid-loaded nanoemulsion을 함유한 hydrogels의 개발, 물리화학적 특성 및 in vitro 연구
을 국소 응용 프로그램 [J]다. J vita Pharmacol, 『 한국정치학회보 』 2019, 71(8):1199-1208.
[40] Panya A, Kittipongpittaya K, Laguerre M, et 상호작용을 알다. 사이 α-tocopherol and rosmarinic 유제의 산 및 그 알킬 에스테르류:시너지 제, 첨가제 또는 길항 제 효과? [J]다. J Agric 음식 화학, 2012, 60(41):10320-10330.
[41]Kittipongpittaya K, Panya A, Phonsatta N, 그 외.rosmarinic acid와 항산화 상호작용에 미치는 환경 pH의 영향 α-tocopherol 오일인 워터 (oil-in-water, O/W) 유제 [J]다. J Agric 음식 화학, 2016년, 64 (34):6575-6583.
[42] Mirchandani Y, Patravale V B, Brijesh S. Solid 친수성 약물용 지질 나노입자 [J.J 제어 해제, 2021, 335:457-464.
[43] 마두레이라 A R, 캄포스 D A, 올리베이라 A 외.에 대한 통찰력을 the protective 역할 of 고체 지질 나노 입자 모의 위장에 노출되는 동안 rosmarinic acid 생리활성에 대하여 조건 [J]다. Colloids 서핑 B Biointerfaces, 2016년,139:277-284.
[44] 쿠로이 C, 루이 I, 라제쉬 R 외.Multiple-component dual-phase 고체 lipid 나노 입자 with conjugated transferrin을 이용한 신경세포 사멸에 대한 항산화물질과 신경성장인자 형성 (J.J Taiwan Inst Chem E,2020, 110:140-152.
[45] Chaiyana W, Anuchapreeda S, Somwongin S, et 지방층 알다. 배달 향상 of 자연 노화방지 화합물 에서 Ocimum 생 텀 Linn다. 추출 nanostructured에 의해 lipid 캐리어 [J]다. Pharmaceutics, 2020, 12(4):309.
[46]Cai Y, Qi J, Lu Y 등.고분자 미셀의 in vivo 운명 (J.Adv 약물 Deliv Rev,2022, 188:114463.
[47] Arranz E, Villalva M, 구리시 A, et al. 단백질 행렬 보장 안전 and 기능 배달 of rosmarinic 마조람 (Origanum majorana) 추출물의 산 [J.J Sci Food Agric, 2019, 99(5):2629-2635.
정 [48] C H, 융 W, 금나나 H, et al. 파생 된 나노 입자 from the 자연 antioxidant rosmarinic 산성을 개선시 킬 급성 inflammatory 장 disease [J]다. ACS Nano, 2020, 14(6):6887-6896.
[49] 류 M, 류 S, 주 X 외.Tanshinone IIA-loaded 미셀이 기능화되었습니다 with rosmarinic 산성: A 소설 동맥경화증 치료를 위한 시너지 항염증 전략.JPharm Sci, 2022, 111(10):2827-2838.
[50]Ding D W, 주 Q D. 최근 PLGA 마이크로/나노입자의 발전이 있었다 을 the 배달 of 바이오acromolecular therapeutics [J.Mater SciEng C, 2018, 92:1041-1060.
[51] 카리미 M, 가세미 A, 사한디 잔가바드 P 외.스마트 마이크로/나노 입자 in stimulus-responsive 마약/유전자 배달 시스템 [J]다. Chem Soc Rev, 2016년, 45 (5):1457-1501.
[52]다 실바 S B,아모림 M, 폰테 P 등이 있다.…의 천연 추출물 chitosan nanocarriers for rosmarinic acid 약물 전달 [J.Pharm Biol, 2015, 53(5):642-652.
[53]다 실바 S, 페레이라 D, 핀타도 M 등.rosmarinic acid ocular delivery-In vitro test를 위한 Chitosan-based nanoparticles에 대한 자료입니다.IntJ Biol Macromol, 2016, 84:112-120.
[54]Casanova F, Estevinho B, Santos L. Preliminary studies of rosmarinic acid microencapsulation with chitosan and modified chitosan for 국소 delivery [J]다. Powder Technol, 2016, 297:44-49.
[55] 가르시아-멜레로제이, 로페즈-미츠자빌라제이, 가르시아-셀마름제이, 그 외 al. Rosmarinic acid-loaded polymeric 준비 가 되어 있는 나노 입자 에 의해 에너지 nano-emulsion templating:정식 화, 생물 물리학 성격묘사, and in 시험관 연구 [J.재료 (바젤), 2022, 15(13):4572.
[56] Rahimi M, Charmi G, Matyjaszewski K, et al. 최근 in natural and 합성 polymeric 골관절염 치료에 사용되는 약물 전달 시스템 [J].Acta Biomater, 2021, 123:31-50.
[57]Ge L M, Zhu M J, 리X Y, 외.active rosmarinic 개발 acid-gelatin 생 분해 영화 항 산화 and 장기적인 항균 활동 [J]다.식품 Hydrocoll, 2018, 83:308-316.
[58] Huerta-Madronal M, Caro-Leon J, Espinosa-Cano E 외.키토산-로스마린산은 항산화, 항염증제와 결합한다 and photoprotective 속성 [J]다.Carbohydr Polym, 2021, 273:118619입니다.
[59] 장제이, 왕 L Q,탄 W Q, et al.chitosan-rosmarinic의 준비 acid derivatives with 향상 된 항 산화 and 항 염증 activities [J]다.Carbohydr Polym, 2022, 296:119943입니다.
[60] Yucel C, Ş eker Karatoprak G. 개발 및 평가 of the antioxidant activity liposomes의 그리고 nanospheres 포함하는 rosmarinic acid [J]다. 「 Farmacia 」, 2017, 65(1):40-45.
[61] Yucel C, Ş eker Karatoprak G, 드 ğ im İ T. 노화 방지 정식 화 of rosmarinic acid-loaded ethosomes 그리고 리포좀 [J.J Microencapsul, 2019, 36(2):180-191.
[62] Baranauskaite J, 압록강 G, Corapc ı o ğ lu G, et 알다. Liposomal 법인 설립 to 개선 해산 및 oregano (O. onites L.) [J]에서 추출한 rosmarinic acid와 carvacrol의 안정성.Biomed Res Int, 2018, 2018:6147315.
[63] Subongkot T, Ngawhirunpat T, Opanasopit p. 개발 ultradeformable의 liposomes with 지방이 많은
향상된 dermal rosmarinic acid 전달을위한 산 [J]다.제약학, 2021, 13(3):404.
[64] 악사미자 A, 폴리도리 A, 플라손 R 외.포함 복합체 (inclusion complex) of rosmarinic acid 로 beta-cyclodextrin: 한 열역학적 and structural 분석 에 의해 NMR 그리고 모세 관 전기 영동 [J]다. Food 화학, 2016, 208:258-263.
[65] Budhiraja A, Dhingra G. 개발 그리고 성격 묘사 of a 소설 antiacne niosomal 젤 rosmarinic acid의 [J].Drug Deliv, 2015, 22(6):723-730.
[66] 황 J H, 첸 P X, 로저스 M A 외.조사 인지질 effect on the bioaccessibility 동적인 위장관 in vitro 모델을 통해 rosmarinic acid-phospholipid complex의.제약학, 2019, 11(4):156.
[67] 비 에이라 L C, 모레 이라 C P S, 카스트로 B F M, et al. Rosmarinic acid intravitreal implants:A new therapeutic approach for ocular neovascularization (영어) [J]다.Planta Med, 2020, 86(17):1286-1297.
[68]Fateminasab F, Bordbar A, Shityakov S 외.분자 사이에 복잡에 대한 통찰력을 포함 형성 β고 γ-cyclodextrins 그리고 rosmarinic 산은다 [J다]J 몰 Liq, 2020, 314:113802.
[69] Veras K S, Fachel F N S, Delagustin M G, et 알다. Complexation of rosmarinic acid hydroxypropyl-와 β-cyclodextrin과 메 틸-β-cyclodextrin:2 ∶ 1 복합체의 형성 항 산화 활동 [J]을 향상시 켰다.J Mol Struct, 2019, 1195:582-590.
[70] 메드론 호브, 발렌테 AJ M, 코스타 P 외.M. Valente, A, 코스타, P. 포함 complexes of rosmarinic acid 그리고 cyclodextrins: Stoichiometry, 협회 상수, 그리고 항산화 가능성 [J.Colloid Polym Sci, 2014, 292(4):885-894.
[71] Rodriguez-Luna A, Talero E, Avila-Roman J, et 알다. 준비 and in vivo 평가 건선에 경피적 시술 후 rosmarinic acid 가 함유된 transethosomes 동물 모델 [J]다. AAPS Pharmscitech, 2021, 22(3):103.
[72] Zhao Yuxia, Chen Yingqian.로즈마리산은 신생쥐의 허혈성 뇌손상을 AMPK/mTOR 경로를 통해 완화시킨다 [J].한방의학, 2021, 52(22):6897-6903.
[73] 아타나소프 A G, 조체프 S B, 디르쉬 V M 외.약물 발견에 천연 제품:진보와 기회 [J].Nat Rev Drug Discov, 2021, 20(3):200-216.
[74]Maher P. 신경 퇴행성 치료를 위한 플라보노이드의 가능성 질병 [J]다. 정수 J Mol Sci, 「 소비자학연구 」 2019, 20(12):3056.
[75] 궈샤오보, 쑤루루, 장리후안 등.쥐에서 rosmarinic acid의 대사산물 및 대사경로 분석 (J.대한한의학회지 2019년, 44(21):4704-4712.
[76] 왕 X이, 취안 X,리 X 등.rosmarinic acid 및 혈장 내 두 가지 생리활성 대사산물의 신속 결정 of 쥐 by LC-MS/MS. and application to 한 약물 study [J]다. Biomed Chromatogr, 2021, 35(2):e4984.
[77] 엄마 B, Wang Y B, 장 Q, et al. LC-MS-MS에 의한 Herba Isodi Rubescentis 추출물로부터 oridonin, ponicidin 및 rosmarinic acid의 동시 측정 rat plasma [J.J 크로마토그 Sci, 2013, 51(10):910-918.
[78] 류 Y,리 X,리 Y 등.danshensu, rosmarinic acid, cryptotanshinone, tanshinone IIA의 동시 결정, tanshinone 나는 and dihydrotanshinone 나는 by 액체 chromatographic-mass spectrometry and the rats의 약리작용에 적용 [J]다.J Pharm Biomed Anal, 2010, 53(3):698-704.
[79]Wang J X, Li G Y, Rui T Q 등이 있다.rosmarinic의 약리작용 acid in 쥐 by LC-MS/MS: 절대 bioavailability and 복용 량 비례 [J]다. RSC Adv, 2017, 7(15):9057-9063.
[80]Qiang Z, YeZ, Hauck C 등.rosmarinic acid의 투과성 in 일 뿐 vulgaris and ursolic acid in Salvia officinalis는 Caco-2세포 단층 전체에 걸쳐 추출한다 [J]다.J Ethnopharmacol, 2011, 137(3):1107-1112.
[81] 양 J H, Zhang L, Li J S, et al. 향상 된 산화 스트레스에 대한 경구 생체 이용성 및 예방 효과 및 간 손상 of an 기름 솔루션 containing rosmarinic 산-인지질 복합체 [J].J Funct Foods, 2015, 19:63-73.
[82] 관 H Q, 루 o W B, 바오 B H 등.종합적인 검토 of rosmarinic 산성: 에서 phytochemistry 약리학과 그 새로운 통찰을 위하여 [J.분자, 2022, 27(10):3292.


 영어
영어 프랑스
프랑스 스페인
스페인 러시아
러시아 한국
한국 일본
일본




