Ginsenoside Rg1 Rb1 Rg3에 Stduy
약리학은 체내에서 약물의 흡수, 분포, 대사 및 배설의 과정을 연구하는 학문이다.이는 약물의 형태와 작용기전을 연구하는 관건이다.약물의 약리작용을 이해해야만 약리작용의 분자메커니즘을 철저히 탐구할수 있다.
Ginsenosides are the ma에서active ingredients 에서the precious Chinese medicinal herb ginseng. They have the functions 의enhancingmemory [1], boosting immunity [2-3], improving blood vessels [4], regulating endocrine secretion [5], delaying aging [6] 그리고fighting tumors [7]. In recent years, the pharmacokinetic researchof ginsenosides has become a hot topic of concern at home 그리고abroad. A review is now given on the pharmacokinetics of ginsenosides 에서the body 그리고the factors affecting them.
여러 ginsenosidemonomer의 약리작용 1
인삼은 한약재로서 약리학적 효과가 입증된지 오래지만, 인삼 에서생체 실험상황에 대한 연구는 아직 걸음마 단계이며, 현재 대부분의 연구는 ginsenosidemonomer의 약리작용에 초점을 맞추고 있다.
1.1 ginsenoside Rg1의 약효
Ginseng sapon에서Rg1can easily pass through the intestinal barrier 그리고is absorbed 에서a time-dependent manner throughout the small intestine [8]. Feng Liang et al. [9] studied the pharmacokinetics and metabolites of 인삼saponin Rg1 in 쥐후intravenous injection and oral administration. After oral administration to rats, the amount of ginsenoside Rg1 metabolites in the body exceeds that of the parent drug. Four substances, ginsenoside Rg1, Rh1, F1 and protopanaxatriol, were detected in the plasma, and their tmax were 0.92, 3.64, 5.17 and 7.30 h, respectively. and the MRTs were 2.68, 5.06, 6.65 and 5.33 h, respectively, and the AUC0-t values were 2363.5, 4185.5, 3774.3 and 396.2 ng·h·mL-1, respectively. After intravenous administration, ginsenoside Rg1 was mainly in 의original form in the 쥐body, 와only a small amount of metabolites. Three substances, ginsenoside Rg1, Rh1 and F1, were detected in its plasma, 와t1/2β of 3.12, 5.87 and 6.87 h, respectively, and MRT of 1.92, 5.99 and 7.13 h, respectively, AUC0-t were 1454.7, 597.5 and 805.6 ng·h·mL-1, respectively. Lee et al. [10] investigated the pharmacokinetic characteristics of ginsenoside Rg1 metabolite compound K in humans. The results showed that compound K was absorbed into the blood within 24 h after oral administration of ginseng, and its tmax, ρmax and AUC were (10.76 ± 2.07) h, (27.89 ± 24.46) ng·mL−1 and (221.98 ± 221.42) μg·h·mL−1, respectively. The 흡수of compound K by the 인간body is not affected by the intestinal flora, but its pharmacokinetic parameters are related to the conversion rate of the intestinal flora in each subject and there are individual differences.
1. 진세노사이드 Rg2의 약효 2
Ginsenoside Rg2, along with ginsenoside Rg1, is a triterpene ginsenoside and a candidate drug for the treatment of cardiovascular and cerebrovascular diseases. It has two isomers, R and S. The AUC of the different isomers of ginsenoside Rg2 in rats is proportional to the dose (intravenous injection: 10, 20, 50 mg·kg-1) and is consistent with a one-compartment open model. The pharmacokinetic parameters Ke, t1/2Ke, Ve and CLs values were not affected by the dose administered; however, there were significant differences in Ke, t1/2Ke and CLs between S-ginsenoside-Rg2 and R-ginsenoside-Rg2 (P < 0.05) [11]. Gui et al. [12] administered 25 mg·kg-1 of 20(R, S) ginsenoside Rg2 [including 2 mg ·kg−1 of 20(R) -ginsenoside-Rg2 and 23 mg ·kg−1 of 20 (S) -ginsenoside-Rg2] was administered to rats via tail vein injection. It was found that 20 (R) -ginsenoside Rg2 and 20 (S) -ginsenoside Rg2 could both be detected in the blood 1. 5 h after injection. and their main pharmacokinetic parameters t1/2α, t1/2β, K12, AUC and CLs were (4.024 6 ± 0.008 7) and (3.724 2 ± 0.045 9) min, (71.1999 ± 3.1586) and (38.4414 ± 1.1134) min, (0.0997 ± 0.157) and (0.0942 ± 0.0358) min-1, (197.7176 ± 5.1766) and (1092.5109 ± 83.0747) μg·min·mL-1, (0. 126 4 ± 0. 000 3) and (0. 023 2 ± 0. 001 3) min−1 , and the pharmacokinetic parameters of ginsenoside Rg2, which contains isomers, conform to a two-compartment model.
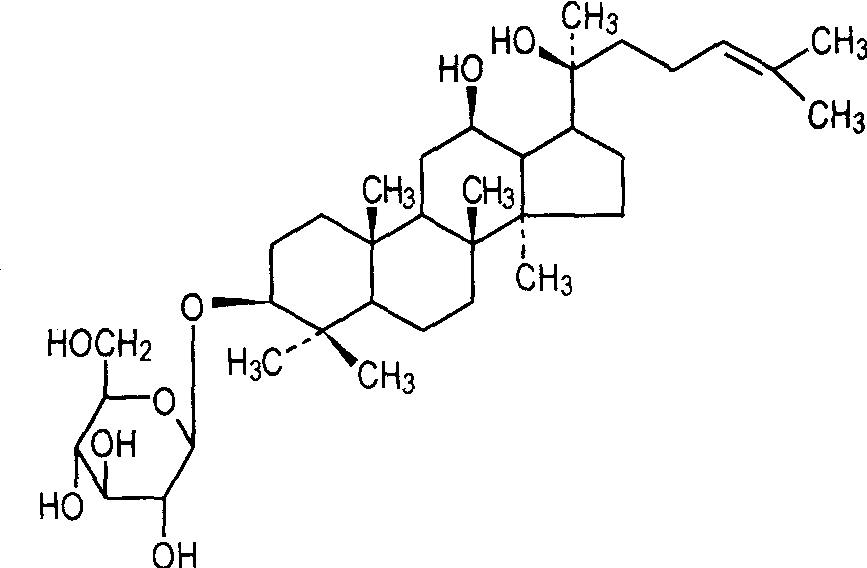
1. ginsenoside Rg3의 약효 3
ginsenoside Rg3를 근육내로 주입한 후 (1.5 mg·kg-1), 쥐의 각 기관에서의 함량분포는 내림차순으로 폐>비장 >심장 >신장 >간이 [13]다.Cai 등 14)은 LC-ESI-MS를 이용하여 쥐 혈장 내 ginsenoside Rg3의 약리작용과 그 체외대사산물을 연구하였다.경구 (50 mg·kg-1) 투여든 정맥 (5 mg·kg-1) 투여든 쥐 소변에서 Ginsenoside Rg3는 검출되지 않았다.그러나 Rg3는 정맥주사 후 1.5시간 이내에 혈액에서 검출될 수 있으며, 빠르게 대사된다 (대사반감기 14분).ginsenoside Rg3의 대사에 대한 추가적인 연구는 위장관 환경을 모사하여 in vitro에서 수행하였다.주요 대사산물은 hydroxyl 그룹을 포함하는 protopanaxadiol 이며, 대사산물로 인식되는 Rh2와 protopanaxatriol은 검출되지 않았다.동시에 ginsenoside Rg3는 주로 간에서 산화 반응을 거친다는 것을 발견했습니다.16시간 후, 쥐간 소솜 S9은 ginsenoside Rg3를 아글리콘으로 산화시켰으며, 이를 cytochrome P450에 의해 24,25-에폭사이드로 산화시켰다.
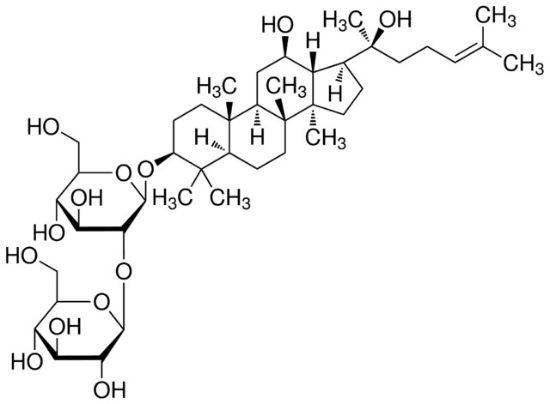
1. 진세노사이드 Re의 약효 4
Liu et al. [15] studied the pharmacokinetics of ginsenoside 회신in humans. After oral administration at a dose of 200 mg·kg-1, the tmax and t1/2 of ginsenoside Re were (1.19 ± 0.44) and (1.82 ± 0.75) h, AUC0-t and AUC0-∞ were (2. 476 ± 2. 281) and (2. 699 ± 2. 284) μg · h · L-1, respectively, ρmax was (0. 939 ± 0. 549) μg · L-1, CL/F was (124 054 ± 84 725) L·h-1. The metabolites of ginsenoside Re in urine were further studied, and three metabolic pathways of ginsenoside Re were inferred: ① Re→Rg1→F1→PPT, ② Re→Rg2→Rh1→PPT, and ③ Re→Rg1→Rh1→PPT. In addition, Joo et al. [16] found that ginsenoside extract can promote the absorption of ginsenoside Re. Ginsenoside Re was administered orally at doses of 10 mg·kg-1 and 50 mg·kg-1, the absolute bioavailability of ginsenoside Re in ginseng saponin extract in rats (0.33% and 0.75%) was higher than that of its monomer administered orally (0.28% and 0.19%).
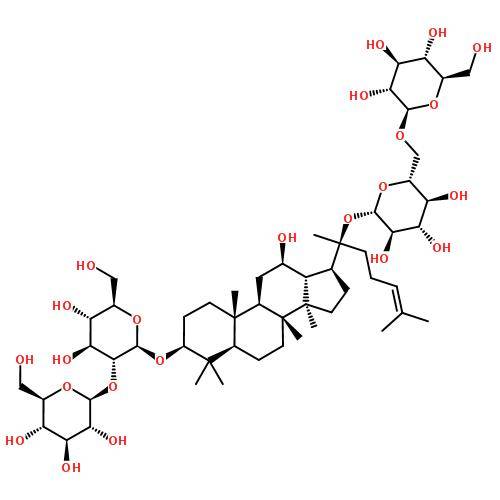
ginsenoside Rb1의 약효 1.5
Ginsenoside Rb1은 주요 protopanaxadiol saponin이다.Qian 등 17)은 쥐의 혈액, 대변 및 소변에서 ginsenoside Rb1의 대사산물을 연구하였다.ginsenoside Rb1의 정맥 투여 (5 mg·kg-1)는 주로 산화에 의해 쥐 체내에서 대사된다;ginsenoside Rb1을 경구 투여 (100 mg·kg-1) 한 후, Rd, Rg3, F2, Rh2, C-K 등의 대사산물이 쥐의 배설물에서 검출되었다.그리고 쥐의 장에서 Rb1의 대사경로는 Rb1 → Rd → Rg3또는 F2 → Rh2 또는 C-K → ppd로 추측된다.쥐의 오줌에 들어있는 대사산물은 대변에 들어있는 대사산물과 비슷하다.경구 투여와 정맥 투여의 대사산물의 차이는 ginsenoside Rb1은 주로 위장관에서 당 그룹을 제거하여 대사된다.
1. ginsenoside Rh2의 약리작용 6
Gu 등 (18)은 쥐를 대상으로 ginsenoside Rh2의 분포를 조사하였다.ginsenoside Rh2 (3 mg·kg-1)를 단일 경구 투여 후, 간에서 가장 높은 농도가 발견되었고, 심장, 비장, 위 및 신장의 농도는 혈중 농도와 유사하였다.난소, 부신, 지방에는 소량이 분포되어 있었고, 뇌, 피부, 근육, 고환에서는 Rh2가 검출되지 않았다.
1. ginsenoside Rd의 약리작용 7
Ginsenoside Rd (10 mg · kg-1) 정맥 주사로 투여 되는 인간의 몸으로, 그리고 나중에 피크 값이 0. 5 h에 도달 했, 한 ρ 맥스 (2 841.18 ± 473.03) ng · mL-1과 t1/2는 2. (19 입니다.29일 ± 3. 44) h, AUC0-t는 (27 161. 63 ± 8개 116. 88) ng · h · mL-1, 그리고 추가 연구를 통해 인삼 saponin Rd를 경구 투여하든 정맥 주사하든 Rg3, Rh2, Rd, Rb1과 같은 대사산물이 쥐의 오줌에서 검출될 수 있다는 것이 밝혀졌다 [19].Wang 등 (20)은 정맥 (0.2 mg·kg-1) 및 경구 (2 mg·kg-1) 투여를 이용하여 개에서 ginsenoside Rd의 약리작용을 조사하였다.개에서 정맥 및 경구 투여 후 ginsenoside Rd의 AUC는 각각 (76,451.1 ± 15,874.8) 및 (1,930.3 ± 647.4) ng·h·mL-1 이었으며 절대 경구 생체이용률은 0.26%였다.
한약복합제 ginsenosides의 약리학적 연구 2
중의약 복합제는 중의약 이론의 정수이며, 현대 중의약 연구의 중점과 열점입니다.최근 연구자들은 화합물 중의 진세노사이드의 약리작용에 대해서도 연구해왔다.장지 등 [21]은 생마이인 (인삼, ophiopogon japonicus 및 schisandra chinensis로 구성된 한약재 복합 조제로 인삼을 주성분으로 함)의 인체에서의 약리적 특성을 연구하였다.12명의 건강한 지원자들에게 생마이인 300 mL를 단일 경구 투여한 후, ginsenosides Rg1과 Re의 약리 프로필은 모두 1 구분 모델을 따랐다.
Rg1과 Re에 대한 평균 피크타임 tmax는 (4.86 ± 1.07)과 (4.75 ± 1.각각 4일) h, 위에 올 랐고, 평균 피크 농도 ρ 맥스 (26일었다.33 ± 12.74)과 (43.32 ± 16.각각 47) μ g · mL-1이다.제거 반감기 t1/2ke는 (7.99 ± 4.63)과 (7.91 ± 4.56) h, 각각 정리 CL은 (2.73 ± 2.50)과 (1.23 ± 1.12) mL · h-1 각각, 그리고 겉보기 volume of distribution V는 (31.10 ± 32.26) 및 (11.96 ± 9.각각 40) mL.AUC0-30은 (205.96 ± 114이다.57)과 (338.73 ± 89이다.10) μ g · h · mL-1, 각각이다.인삼 사포닌 Rg1과 Re인체에서 1차 운동 흡수 및 제거를 받는다.한편, 린리 등 [22]은 복분자인 인삼이 ginsenosides Rg1, Re, Rb1 및 Rd의 흡수에 미치는 영향을 연구하기 위해 쥐의 장내 sac 모델을 이용하였으며, 그 결과 단일성분과 비교하여 복분자인 저용량군 (0.281 mg · mL-1)은 ginsenosides Rg1, Re, Rb1 및 Rd의 흡수를 촉진 할 수 있으며, 화합물 중간 투여군 (0.563 mg · mL-1)과 고용량군 (1.125 mg · mL-1)은 4가지 성분의 흡수에 유의한 차이를 보이지 않았으며, 복합투여량이 증가할수록 이들 4가지 성분의 흡수가 억제되는 경향을 보였다.

ginsenosides의 약리작용에 영향을 미치는 인자 3
약물의 흡수와 유통은 매우 복잡한 과정이며 이에 영향을 미치는 요인으로는 피험자의 종별 차이, 약물의 용량 형태, 투여 경로, 투여되는 용량 등이 있다.
3. 1 과목
Due to species differences among the test animals, the pharmacokinetic models of ginsenosides in different test animals are different. Gu et al. [18] studied the pharmacokinetic of ginsenoside Rh2 in dogs and rats. The pharmacokinetic model of ginsenoside Rh2 after intravenous injection in Beagle dogs (0.1 mg·kg-1) was a three-compartment open model, while in rats (0.1 mg·kg-1) it was a two-compartment model.
3. 2 약물 복용량 형태
복용량 형태는 시험 약물의 약리작용에 상당한 영향을 미친다.약물 용량 형태의 변화는 약리학적 변수의 변화로 이어질 것입니다.인삼 사포닌 조제도 예외는 아니다.Rode Feng 등 [23]은 쥐의 다양한 장분절에서 체외방출율과 ginsenoside Rd 고체지질 나노입자 (Rd-SLN)의 흡수특성을 조사하고, 이를 ginsenoside Rd 단량체와 비교하였다.120시간 이후 Rd-SLN의 누적약제방출율은 (89.6 ± 1.6)%인 반면, ginsenoside Rd 대조액은 12시간 이후 동일한 매질에서 거의 완전히 방출 (97.21 ± 1.19%) 되었으며, 쥐의 장분절에서 Rd-SLN과 Rd의 흡수율도 차이를 보였다.
십이지장과 공장 분절에서 둘의 흡수는 유의한 차이가 없었으며 회장 및 대장 분절에서 둘의 흡수율의 차이는 유의하였다.동일한 용량 조건에서 Rd-SLN 군의 최고 혈중 농도는 Rd 군에 비해 유의하게 높았으며 t1/2 및 MRT는 유의하게 연장되었다.전자의 AUMC, AUC0-t, AUC0→∞는 각각 후자의 약 2배, 1.5배, 2배였다.그 결과 Rd-SLN은 약물의 방출을 늦추고, 장내 약물의 흡수를 증가시키며, 경구 투여시 생체 이용성을 현저히 향상시키고, 혈액 내 반감기를 연장시키는 것으로 나타났다.또한 Gu 등 (18)은 비글견에서 20(R)-ginsenoside Rh2의 미세화 전후 약리인자 변화를 조사하였다.비글견을 경구 투여 (1 mg·kg-1) 20(R)-ginsenoside Rh2와 그 미분말을 각각 혈중 약물 농도를 샘플링하여 투여 후 0.25, 0.5, 0.75, 1.0, 1.5, 2, 3, 5, 7, 9, 12, 24, 36시간에 검사하였다.그 결과는 다는 것을 보여주 ρ 맥스, AUC와의 micronized 20 (R)-ginsenoside Rh2 원래 마약의 그러 한 두 번,에 관 한 것이었음을 나타내는 micronized 20 (R)-ginsenoside Rh2에서 더나은 장내 유동 적이고을 녹 일 수 있 더 쉽게 피를 입력 합니다.
3. 3 행정노선
Gu 등 (24)은 비글견에서 경구 및 정맥 투여 후 ginsenoside 20(R)-Rh2의 약리변화를 조사하였다.정맥주사 후 ginsenoside 20(R)-Rh2의 약리곡선 (0.1 mg · kg-1)은 3 칸 모델에 부합하였으며, 주요 약리변수인 t1/2, CL 및 auc0-∞는 (8.0 ± 2이다.8) h, (0.1 ± 0.03) L · kg-1 · h-1, (857.0 ± 209.6) ng · h · mL-1, 그리고 긴 말단 제거 반감기로 20(R)-Rh2가 체내에 어느 정도 축적될 수 있음을 시사한다;그리고 경구투여 (1 mg·kg-1) 후의 약리모델은 2 칸 모델이다.주요 pharmacokinetic 매개 변수 tmax ρ 맥스, t1/2, 그리고 AUC0-∞ (130) 260 ± h, (371.0 ± 199.6) ng · mL-1, (5. 8 ± 2. 6) h, (1215.7 ± 598.6) ng · h · mL − 1 입니다.비글견에서 20(R)-Rh2의 흡수가 느린 것은 용해도 및 분산이 잘 되지 않는 것과 관련이 있을 수 있다.또한 P-glycoprotein의 유출과 장내 식물체의 대사작용으로 인하여 비글견에서 약물의 절대생물학적 이용성은 낮은 수준으로 (16.1 ± 11.3)%에 불과하다.따라서 20(R)-Rh2에 대한 투약 형태의 개발은 형질전환을 줄이고 약물의 흡수를 증가시키기 위한 투여 방법을 고려해야합니다.
3. 4 복용 량
현재 연구에 따르면 설정된 투여량 범위 내에서 동일한 구성의 ginsenosides의 경우 투여량 농도가 증가함에 따라 각 투여군의 약리작용변수는 증가하지만 유의한 차이는 없는 것으로 밝혀졌다 (P>0.5일).Deng Yuanhui 등 25명은 12명의 건강한 중국인 지원자를 대상으로 한 번의 정맥 주입 후 ginsenoside-Rd 주사의 약리 특성을 연구하였다.그 결과의 주요 pharmacokinetic 매개 변수 3 복용 량 (10, 40 75 mg · kg-1):ρ 맥스었(2.84 ± 47), (10.48 ±. 74), (19.34 ± 도요타자동차) mg · L-1,와 t1/2 (19.29 ± 1위), (18.41 ± 2. 92), (17.67 ± 비해) h,와 AUC0-t (27.26 ± 8.12), (112.62 ± 24.08), 그리고 (208.36 ± 51.36) mg · h · L-1, 각각이다.ρ 맥스, AUC0-t 복용 량과 좋은 선형 관계, 비례적으로 증가의 복용 량의 증대와 함께 약물이다.선량보정과 자연로그 변환 후에는 분산 분석을 통해 각 파라미터의 세 가지 선량간에 큰 차이가 없습니다.펭잉 (Peng Ying) 등 [26]은 쥐에서 ginsenoside Re의 다양한 용량에 따른 약리적 특성을 연구하였다.세 가지 다른 용량 (20, 30, 40 mg·kg-1)의 ginsenoside Re를 정맥 주사한 후, 세 그룹의 쥐의 약리작용은 모두 이중구획 모델이었다.그 t1/2 α었6.505, 6.817 및 4.499 민, t1/2 β은 28일이었다.96, 30.49 화, 27 화에서 등장.각각 57 min, AUC는 599였다.31, 1 025 쪽.65, 1 415 쪽.각각 7 min · mg · L-1.세 집단의 쥐들의 주요 운동변수는 비슷하였으며, AUC는 투여량의 증가에 비례하여 증가하여 Re의 제거가이 투여량 범위 내에서 선형임을 알 수 있었다.
진세노사이드의 약리연구를 위한 새로운 아이디어 4
4.1대사산물의 약리학적 연구
경구투여는 현재 대부분의 사포닌 화합물의 주된 투여방법이다.경구 투여 후 사포닌 화합물이 장내 균에 의해 쉽게 대사되고, 원래 약물의 혈중 농도가 낮다는 연구 결과가 나왔다.따라서 일부 학자들은 대사산물의 혈중 농도를 측정하여 진세노사이드의 약리작용을 연구하기도 한다.Ren 등 27)은 혈장 내 20(S)-protopanaxadiol (PPD)의 측정을 위한 HPLC-APCI-MS 법을 확립하고 쥐에서 경구 투여 후 PPD의 약리적 특성을 연구하였다.그 결과의 PPD ρ 맥스에 쥐었(130.2 ± 41.5) ng · mL-1 tmax은 (150.0 ± 73.5) 분. 절대의 PPD었(36. 8 ± 12. 4)%, 10배의 prodrugs ginsenosides Rg3 그리고 Rh2, 나타내 PPD이 혈류로 더 쉽게 흡수 다는 것이다.따라서 PPD의 혈중 농도를 측정하면 ginsenosides Rg3 및 Rh2의 약리적 특성을보다 정확하게 반영할 수 있습니다.
4.2 질병 모델에 따른 약리작용
증후군모델에서 한의학의 약리과정은 일반적인 생리동물의 약리과정과 다르다.따라서 한의학의 약리작용을 증후군을 토대로 연구하는 것이 더욱 유익하다.Zhou Wei 등 28은 정상 상태에서 쥐와 뇌졸중의 급성 및 회복 단계에서 gardenoside, ginsenoside Rg1, Rb1 및 notoginsenoside R1을 포함한 Qingnao Xuanqiao Fang의 유효성분의 약리학적 변화를 연구하였다.그 결과 청나오 Xuanqiao ₃의 유효성분인 gardenia, 인삼 saponin Rg1, 노토 인삼 saponin R1은 모두 정상군과 모델군에서 2 칸 개방형이었으며 인삼 saponin Rb1은 1 칸 개방형모델에 일치하였다.4에서 성분의 흡수를 쥐었빠 른, 45분 뒤에 ρ 맥스에 도달하고 있다.gardenoside, ginsenoside Rg1, notoginsenoside R1의 제거는 빠른 반면, ginsenoside Rb1의 제거는 느렸다.다른 모델 동물의 경우, 4가지 성분의 혈중 농도-시간 곡선하에서의 최대 혈중 농도와 면적은, 가장 높은 곳에서 가장 낮은 곳으로 급성 모델군>회복모형>정상적인 그룹이다.약물에 대한 모델군의 생체이용성은 정상군보다 높아 모델동물이 정상동물에 비해 Qingnao Xuanqiao Fang의 흡수가 증가됨을 알 수 있다.
4. 3다 성분 통합 약제
한약의 효과는 다성분 및 다표적 효과의 기전을 가지고 있다.한약의 약리작용과정과 처방을 단일 성분의 약리작용인자에 의해 설명하는 것이 더 일방적이다.따라서 Li Xiaoyu 등 [29]은 panax 노토인삼 사포닌을 모델 약물로 사용하여 맞춤형 중량계수를 갖는 panax 노토인삼 사포닌의 각 성분의 곡선 (AUC0-∞) 아래 면적을 기반으로 하는 통합 약리학 연구 모델을 구축하였다.쥐를 대상으로 Panax noto인삼총사포닌 (300 mg·L-1)을 가반하중과 (10 mg·L-1) 정맥 주사하였고, 쥐 혈장 내 notoginsenoside R1, ginsenoside Rg1, Rd, Re, Rb1의 약물 농도를 LC-ESI-MS를 이용하여 확인하였다.가배지에 의한 투여 후, 총노토삼 사포닌은 쥐의 체내에서 빠르게 흡수되지만, 디올 사포닌 Rb1 및 Rd의 t1/2가 트리올 사포닌 Rg1, Re 및 R1보다 훨씬 많으며,그리고 각 성분의 곡선 (auc0-∞) 하에서의 백분율 영역을 자가정의 가중치 인자로 사용하여 구축한 통합약리연구모델의 결과는 복합동심시간곡선이 가반하중이나 정맥 주사로 투여되는 약물의 제거법칙에 부합함을 보여주었다.파낙스 노토삼 총사포닌은 쥐에서 빠르게 흡수된다.가방과 정맥 투여 후 통합 약제 t1/2와 AUC는 18.88과 19였다.15 h와 25.33, 84.각각 83 mg · h · L-1.이 모델은 고전적인 약리학 모델의 특성을 따르며, 얻어진 파라미터는 한의학의 전반적인 성향을 최대한 특징지을 수 있다.이는 한약재의 특성에 부합되는 약리학 연구를 정립하는데 새로운 연구 아이디어와 방법을 제공한다.
5 전망
Ginsenosides는 다양한 생물학적 활성과 중요한 임상 효능을 가지고 있습니다.이들의 약리학적 효과 및 약리작용에 대한 광범위한 연구가 수행되었고, 일부 성과를 거두었다.하지만, 여전히 개선이 필요한 부분들이 있습니다.
On the one hand, ginsenosides are easily metabolized by the gastrointestinal tract and liver, and their blood concentrations in the body are low and not easy to detect. Therefore, modern high-sensitivity analytical techniques (GC-MS/MS, LC-MSn, LC-NMR, etc.) need to be applied to the detection of ginsenosides in vivo. At the same time, since the substances that exert effects on target tissues in vivo may be their metabolites, attention should also be paid to the detection and analysis of ginsenoside metabolites. On the other hand, pharmacokinetic studies of ginsenosides at home and abroad have only studied the relationship between blood concentration and time from a chemical perspective [15, 21], ignoring the connection with efficacy.
따라서 향후 연구에서는 진세노사이드의 약리작용을 약동학적 지표와 결합하여 동심-시간-효과의 3차원적 관계를 탐구하고 동시에 약리작용과 약동학적 분석 모델을 수립함으로써보다 현실적이고 객관적으로 진세노사이드의 체내약리작용과정을 반영하고 임상적 효능에 일정한 근거를 제시하여야 할 것이다.또한 한약재인 인삼에는 많은 종류의 진세노사이드 (ginsenoside) 가 존재하며, 각 개체의 약리변수가 달라 [30] 인삼의 전반적인 약리작용 및 특성을 특정할 수는 없다.따라서 한의학 이론을 지도하고 대사체학, 단백체학, 유전자칩 등의 현대 실험기법을 접목하여 시스템 생물학 관점에서 한의학의 다중효과 성분에 대한 약리연구를 위한 새로운 방법을 모색해야 한다 [31].
참조:
[1] 장G,LIU A,ZHOU Y, 외. panax 인삼 ginsenoside-rg2 쥐 모델에서 anti-apoptosis를 통해 기억 장애를 보호합니다 혈관성 치매 [J.JEthnopharmacol,2008,115 (3)::한국신학연구소 441-448다.
[2] 유 XT, 왕 S P.ginsenoside에 의한 postop-erative gastric cancer 치료에 대한 임상적 소견 Rg3 결합 with chemo-요법 [J].Chin J Cancer Prev Treat, 2010,17 (10):779-781.
[3] ZHANG Z, 장 B, 정화 X, et 면역이 알다. 강화 Rg3의 효과 암 환자의 시험관 내 말초 림프구에 방사선 치료로 치료 [J.Chin Pharm J, 2004,39(4):261-264.
[4] SUI D Y,YU X F,QU S C, 외. effects of Panax quinquefoli-um 20S-2protopanaxdiol saponins on experimental ventricular re-modeling in 쥐[J].Chin Pharm J,2007,42 쪽 (2):108-112.
[5] 인삼의 성분인 LEE Y,JIN Y,LIM W,et al.A ginsenoside-Rh1 사포 닌, 활성화 에스 트로 겐 수용체 in human 유방암 MCF-7세포 [J.J Steroid Biochem,2003,84 (4):463-468.
[6] 윌리엄 C S, 정 W S, 샐리 K W 외. 진세노사이드 Panax 인삼의 Re는 상당한 항산화 및 antihy-perlipidemic을 보유하고 있습니다 효능 in streptozotocin-induced 당뇨병 환자 rats [J]다.Eur J Pharmacol,2006,550(1-3):173-179.
[7] KIM S E,LEE YH,PARK H J,et al.Ginsenoside-Rs4,a new 인삼 saponin의 종류는 동시에 apoptosis를 유도하며 selec은 인간의 hepato-ma SK-HEP-1세포 European [J]에서 p53과 p21WAF1의 단백질 수준을 효과적으로 상승시킨다.Eur J 암,1999,35 (3): 507-511다.
[8] LI H,SUN J G,XIE H T,et al.Study on absorption mechanism of ginsenoside (진세노사이드) Rg1 사용 rat everted 내장 sac [J].Chin J Clin Pharmacol Ther,2004,9 (5):510-513.
[9]. 풍 L, 후 C J, 유 L Y, 외 ginsen-oside Rg1의 약리작용 그리고 그 대사산물은 쥐 [J.Acta Pharm Sin,2010,45 (5):636-640.
[10] 경구투여 후 인삼의 체내 흡수, distribution 및 대사에 관한 연구 (LEE J,LEE E,KIM D,et al.Studies on absorption, distribution and metabolism of 인삼 in human after oral administration)J Ethnopharmacol,2009,122(1):143-148.
[11] 양 X W,GUI F J,TIAN J M,et al.Pharmacokinetics of ginsenoside-Rg2 쥐에서 [J.Chin Pharmacol Bull,2009,25 (7):967-970.
[12] GUI F J, 양 X W,LI L Y, 외 20의 동시 앙량체 결정 (R)-그리고 20 (S)-ginsenoside-Rg2를 HPLC 법을 이용하여 정맥투여 후 rat 혈장에서 [J.J 크로마토그래피 B,2007,850(1-2):1-6.
[13] 황 Y, 류 J H.Pharmacokinetic 연구 진세노사이드 20 (S)-Rg3의 in rats by HPLC-ELSD[J]에서 등장.J Pr Med Theory,2005,12(9):2564-2566.
[14] CAI Z,QIAN T,WONG R,et al.Liquid chromatography-elec-trospray ionization mass spectrometry for metabolism and pharma-cokinetic studies of ginsenoside Rg3[J].Anal Chim Acta,2003, 492(1-2):283-293.
[15] 류 L, 황 J, 후 X 외 진세노사이드 동시 판정 (G-Re,G-Rg1,G-Rg2,G-F1,G-Rh1) and proto-panaxatriol in human 플라 즈 마and urine by LC-MS/MS and its ap-plication in G-Re in volunteers [J]의 약리작용 연구. J 크로마토그래피 B,2011,22(15):2011-2017.
[16] JOO K,LEE H J,JEON H Y, 외 ginsenoside Re의 약리연구 with 순수 한 ginsenoside Re and ginseng 베리 추출 물에 마우스 사용 초고 성능 액체 크로마토그래피/ 질량분석법 [J.J 제약 바이오메드,2010,51 『 한국정치학회보 』 (1-2):278-283.
[17] QIAN T,JIANG Z H,CAI Z.고성능 액체 크로마-토그래피와 탄뎀 질량 분석기가 rat에 대한 ginsenoside Rb1의 meta-bolic 연구를 위해 적용되었다 [J].Anal Biochem,2006, 352(1):87-96.
[18]. GU Y,왕G J,SUN J. (구 Y.인삼의 항암영양소인 ginsenoside Rh2의 쥐와 개에서의 약리학적 특성 (J.Food Chem Toxicol,2009,47 (9):2257-2268.
[19] YANG L,덩 샤 오 핑Y,XU S,et al.In vivo pharmacokinetic 및 신진대사 연구 (metabolism studies of ginsenoside Rd [J])J 크로마토그래피 B, 2007,854(1-2):77-84.
[20] WANG W,WANG G J,XIE H T,et al.Determination of gin-senoside Rd in 개plasma by liquid chromatography-mass spec-trometry (액체 크로마토그래피-질량 스팩-트로metry) after solid-phase 추출 and its 응용 프로그램 in dog 약리학 연구 [J.J 크로마토그래피 B,2007,852 (1-2):8-14.
[21] JIANG J,LI S,GONG P L,et al.Pharmacokinetics of Shengmaiyin oral solution after a single dose in human [J.액 타 의대 대학 Sci Technol 허정숙, 2007,36(2):272-274.
[22] LIN L,ZU F Y,ZHANG W W, 외. 화합물 적합성이 ginsenoside saponins의 in 체외에서의 흡수에 미치는 영향.턱 J Mod Drug Appl,2010,4 (13):150-152.
[23] LUO D F,YE J T,ZHANGY S,et al.Studies on drug release in.에 대한 연구 vitro and absorption in rat in vivo of ginsenoside Rd 고체 지질 나노 입자다 [J다]Chin Pharmacol Bull, 2009,25 (7):923-926.
[24] 구 Y, 왕 G J,SUN J G, 외 ginsenoside의 약리연구 20(R)-Rh2 LC-ESI-MS [J]의 비글 개에서.Chin J Clin Pharmacol Ther,2006,11 (3):159-163.
[25] DENG Y H,ZENG X,FENG Y,et. pharmacokinetics 및 중국 건강 자원 봉사에서 ginsenoside-Rd injec-tion의 단일 복용 정맥 주사의 허용.Chin J Clin Pharmacol,2009,25 (2):116-120.
[26] PENG Y,WANG S J,PAN W S,et al.Pharmacokinetics of ginsenoside Re in rat [J].J Shenyang Pharm Univ,2006,23 (4):197-200.
[27] REN H C,SUN J G,WANG G J,et al.Sensitive 결정 20 (S)의-프로 토 파나 사 디 올 in rat plasma 사용 HPLC-APCI-MS: 쥐에 대한 약리연구의 응용 [J].J Pharm bi-omed,2008,48 (5):1476-1480.
[28] ZHOU W,SHI R B,SUN J N,et al.Pharmacokinetics of effec-tive fractions of Qingnaoxuanqiao Formula in different rat models [J]다.J 북경부대 Tradit Chin Med, 2008,31 (4):265-268.
[29]. LI X Y,HAO H P,WANG G J,et al.Integrated pharmacokinet-total panax에 함유된 여러 유효성분에 대한 연구 notoginsenosides다 [J다]Chin J Nat Med,2008, 6(5):377-381.
[30] 송 M, 장 S, 수 X 외 동시 결정 LC-MS/에 의한 sub-nanogram에서 3가지 Panax noto인삼사포닌의 복합 Danshen tab의 약리작용을 위한 개 혈장내 MS-lets [J].J 크로마토그래피 B,2010,878 (32):3331-3337.
[31] WANG Z, 엄마 첸 X, X, et 현재 알다. 방법 and ad-vancesin 미생물 metabolom ics[J].Prog Chen, 2010,22(1):163-172.


 영어
영어 프랑스
프랑스 스페인
스페인 러시아
러시아 한국
한국 일본
일본




