골관절염에 대한 인삼추출물 Ginsenoside에 관한 연구
골관절염 (OA)은 노화, 비만, 유전, 변형, 외상, 선천적 관절이상, 관절기형 등 여러 가지 요인에 의해 발생하는 퇴행성 질환이다다.관절연골의 퇴행성 손상과 관절가장자리 및 연골하골의 반응성 과증식이 특징이다.임상증상으로는 서서히 진행되는 관절통, 압통, 뻣뻣함, 관절부종, 제한된 움직임, 관절기형 [1] 등이 있다.현재 OA의 전통적인 치료법으로는 주로 비스테로이드성 항염증제, 글루코코르티코이드, 물리치료 등이 있다.중증 환자의 경우 관절치환술을 요구하는 경우가 많다 [2].따라서 OA 치료에 있어 부작용이 적고 효능이 좋은 약을 찾는 것이 시급한 문제로 대두되고 있다.한의학에 대한 연구가 깊어짐에 따라 인삼은 관절연골 손상과 변성을 예방하고 치료하며, 체외 [3]에서 연골세포를 배양하여 관절연골 결손 회복에 참여할 수 있다는 전망이 밝아 OA 치료에 새로운 사고방식을 제공하였다.
Ginseng (Panax ginseng C. A. Mey.) is 이dried root 그리고rhizome of a perennial herb 에서the family Araliaceae. It is a traditional precious medicinal herb that has been used 에서China for many years [4]. As one of the “Three Treasures of Northeast China”, ginseng has pharmacological effects such as anti-inflammatory, anti-oxidant, anti-depressant, anti-Alzheimer's 병, 항동맥경화증, 항oa 병이며 사용역사가 길고 약효가 극히 높다 [5].인삼의 주요 약리학적 활성 성분인 진세노사이드는 질병 치료에 핵심적인 역할을 한다.연구에 따르면 ginsenosides는 염증 인자를 억제하고 연골세포 사멸과 기질 손상을 감소시키며 연골세포 회복을 촉진하여 OA [6]에 치료 효과를 발휘함으로써 관절 통증을 개선하고 손상된 연골을 회복시키는 것으로 나타났다.인삼의 약리학적 활성은 연구가 잘 되어 있지만 진세노사이드에는 많은 종류가 있다.어떤 ginsenosides 가 OA에 치료 효과를 가질 수 있는지, ginsenoside 단량체의 복합 응용이 효과적인지 여부, 목표한 특정 단백질 및/또는 거대 분자와 같은 구체적인 치료 작용 기전 등에 대해서는 아직 완전히 밝혀지지 않았다.본 글에서는 최근 OA 치료에 대한 ginsenosides의 연구 및 진행 상황을 살펴봄으로써 OA 치료에 대한 ginsenosides의 임상적 적용을 위한 기초자료를 제공하고자 한다.

진세노사이드 (Ginsenosides)와 이들의 분류 1
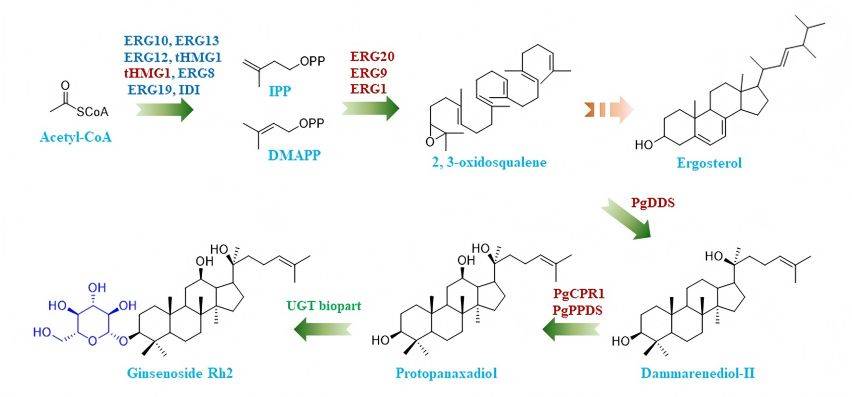
스테로이드 유사 사포닌이라고도 하는 진세노사이드 (G)는 인삼의 고유 성분이며 일반적으로 Rx로 표시한다.현재 인삼식물의 뿌리, 줄기, 잎, 꽃, 열매에서 150개 이상의 자연 발생 진세노사이드를 분리할 수 있다.이러한 진세노사이드는 골격 유형에 따라 4가지로 구분할 수 있다.이들은 모두 테트라사이클릭 소수성 구조를 공통으로 가지고 있지만, 당 부분은 다르다.서로 다른 당 분자는 4개의 주요 사슬의 다른 영역에 부착되어 독특한 진세노사이드 단량체 분자를 생성하며 (표 1), 이는 서로 다른 약리학적 활성을 결정한다 [7-9].
Of these four ginsenosides, protopanaxadiol-type and protopanaxatriol-type ginsenosides account for more than 90% of total ginsenosides 에서ginseng and have stronger activity. They are the main active ingredients of ginsenosides and are also the focus of current research. Among these, G Rb1, G Rg 1, G Rg3, G Rd, G Re, G Rh1 and G Rh2are the most frequently studied [10]. This study provides a detailed introduction to the research progress ginsenoside의monomers such as GRb1, GRg1, G Rg3 and G Ro, and monomers in combination and traditional Chinese 약formulas for the treatment of OA.
2 OA 위험요인 및 치료방법
OA 발전에 기여한 요인 2.1
OA는 관절염의 가장 흔한 형태 중 하나로서 연령, 성별, 비만 등 개인적 요인을 포함하여 여러 가지 요인의 영향을 받는다.연구에 따르면 65세 이상 인구의 1/3이 OA의 영향을 받고 있으며 [11], 여성에서 발병률이 50세 이후 크게 증가하는데 [12], 이는 주로 폐경 이후 에스트로겐의 감소로 인해 여성에서 관절연골의 분해가 증가하기 때문이다 [13].또한 스포츠 부상은 관절 구조에 이상을 초래하여 연골 소실의 위험을 증가시키며 OA [14]의 발달을 직접적으로 초래할 수 있다.관절에 가해지는 기계적 스트레스는 관절세포에서 염증성 인자의 발현을 증가시키며, OA 연골의 이화과정 [15] 에도 일부 원인이 있다.OA의 발달은 신진대사 [16, 17], 유전, 면역 [18] 등의 요인과도 밀접한 관련이 있다.
2.2 OA의 처리
현재 OA를 치료하는 다양한 기술적 방법이 있습니다.물리치료 (운동치료 및 정형외과적 기기로 보완된 환자교육 포함) [19] 외에도 경구약물치료, 관절내 주사, 말기수술 [20] 등을 통해 통증완화, 질병의 진행지연, 기능향상도 가능하다.
Standard drug therapy includes pain and 염증control drugs such as non-steroidal anti-inflammatory drugs, opioid analgesics and intra-articular corticosteroids, as well as symptomatic relief of arthritis such as oral glucosamine sulfate, chondroitin sulfate, dexamethasone, soybean and avocado unsaponifiables extracts, and intra-articular hyaluronic acid injections [21]. In addition, some studies have shown that Chinese 허 브medicines such as Gan Cao Tang also have a certain effect in the treatment of OA [22]. However, drug therapy has little effect in severe cases, and surgery is the only option. The most common and most effective is joint replacement [23]. Of course, traditional Chinese medicine methods such as acupuncture [24], massage [25], physiotherapy, Chinese herbal plaster, Chinese herbal fumigation, Chinese herbal application [26], Chinese herbal ironing and targeted Chinese herbal medicine can also be used to slow the progression of OA [27].
OA에 대한 ginsenosides의 치료 효과에 대한 연구 진행 3
3.1 진세노사이드 Rb1
Ginsenoside Rb1 (G Rb1)은 주로 파낙스속에 속하는 파낙스인삼에서 유래한다.인삼의 줄기와 잎에 들어있는 함량은 뿌리, 무좀, 뿌리털에 들어있는 함량보다 훨씬 낮다.GRb1은 트리테르펜 사포닌으로 40개 이상의 개별 진세노사이드 중 가장 풍부하다.노치 신호경로, NF-KB 신호경로 [9] 등 염증성 사이토카인의 발현을 억제함으로써 항염증, 항세포사멸 및 신경보호 효과를 발휘할 수 있는 것.
GRb1 can exert a protective effect on articular cartilage by inhibiting the expression of inflammatory cytokines. Cheng et al. [28] constructed a cartilage OA model by stimulating with interleukin (IL)-1, and then administered a certain amount of GRb1 for index detection. It was found that GRb1 could inhibit the production of inflammatory factors such as matrix metalloproteinases (MMP)-13, cyclo-oxygenase-2 (COX-2), prostaglandin E2 (PGE2), inducible nitric oxide synthase ( iNOS) and nitric oxide (NO), and reduces the degradation of Collagen II and proteoglycan (ACAN) induced by IL-1β in 인간articular chondrocyte, which indicates that the mechanism of action of GRb1 may be similar to that of non-steroidal anti-inflammatory drugs, which can relieve the symptoms of OA by inhibiting the expression of COX-2 and PGE2.
This effect was also verified in an OA rat model. Ara-vinthan et al. [29] found that GRB1 may inhibit the levels of MMP13 and COX-2 mRNA and inhibit interferon (Interferon gamma, IFN-) monocyte chemoat-tractant protein-1 (MCP-1)/chemokine ligand-2 (CCL-2), IL-1P and IL-6 inflammatory cytokines/chemokines expression, thereby preventing cartilage degradation, and thus helping GRb1 exert anti-inflammatory effects on MIA-induced ovarian OA rats. Gao Zhi [30] established an 골관절 염model by cutting the anterior cruciate ligament of the right knee joint of rats and treated the rats based on different doses of GRb1. The results showed that GRb1 significantly reduced the number of white blood cells and lymphocytes in the blood of model rats, and in a concentration-dependent manner, it reduced the levels of TNF-α and IL-1β in rat serum, and also reduced the expression of MMP-9, MMP-13 and AD-AMTS-5 expression, while increasing Collagen II and Aggrecan expression in cartilage tissue, indicating that G Rb1 can inhibit cartilage degradation by inhibiting inflammatory responses and the synthesis of MMPs in joint tissue, and has a good therapeutic effect on osteoarthritis induced by anterior cruciate ligament transection.
G Rb 1 has multiple mechanisms of action in the treatment of OA, possibly through the Notch signaling pathway and the NF-KB signaling pathway. For example, Wang Wei [31] found that GRb1 can reduce IL-1β-induced expression of type II collagen and MMP-13 in cells, while also reducing the expression levels of Notch1 and JAG1 after induction, indicating that the protective effect of GRb1 on chondrocytesmay be achieved by inhibiting the expression of MMP-13 and activation of the Notch signaling pathway. In addition, Hossain et al. [32] constructed an OA rabbit model and found that GRb1 can prevent chondrocyte apoptosis, inhibit the production of reactive oxygen species (ROS) in chondrocytes, down-regulate the p38/MAPK and PI3K/AKT signal pathways to prevent the expression of MMPs and balance the expression of collagen type II and proteoglycans, and activate NF-KB signal transduction to exert a protective effect on chondrocytes, thereby being used to treat OA.
진세노사이드 Rg1 3.2
진세노사이드 Rg1 (G Rg1)최초에 중국 약초인 인삼의 뿌리와 줄기에서 추출된다.30개의 탄소 원자를 가진 트리테르펜 담마라네 고리 유도체이며 글루코코르티코이드 스테로이드와 유사한 구조이다.글루코코르티코이드 수용체에 결합함으로써 글루코코르티코이드 약물과 유사한 항염증 효과를 발휘할 수 있다.황유민 [33]은 전방십자인대 절제 (ACLT)와 MIA 관절강 주입을 통해 쥐에서 OA 모델을 제작하였고, G Rg1이 IB의 인산화를 억제함으로써 NF-KB의 활성화를 억제하여 연골세포인 MMP-13과 PGE2의 합성을 감소시켜 연골 보호효과를 발할 수 있음을 발견하였다.
또한 G Rg1은 조골세포 사멸을 억제하고 조골세포 증식을 촉진하여 조골세포 보호 효과를 발휘하므로 OA의 치료에 잠재적인 가치가 있다.Duan Chao et al. [3]은 고정직관 석고를 6주간 모델링 하는 방법을 사용하여 클리닉에서 볼 수 있는 것과 유사한 인간 OA의 토끼 모형을 성공적으로 확립하였다.GRg1이 토끼무릎 OA 관절연골세포의 세포사멸에 미치는 영향을 관찰한 결과, 일정 용량의 GRg1이 연골조직에 긍정적인 보호효과가 있음을 확인하였다.이는 연골세포의 주요 인자인 Bax/Bcl-2의 발현비를 조절하고 Caspase-3의 발현을 하향조절함으로써 연골세포의 과도한 사멸을 효과적으로 억제하고 연골조직의 진행성 파괴를 방지할 수 있다.게다가, 황 et al. [34] 다는 것을 발견 GRg1-pretreated IL-1 β-induced chondrocytes 또한 Bcl-2 표현을 촉진, Bax 활동을 억제하고 CytC 석방을 줄이고 Caspase-3 활성화.또한 TIMP-1발현을 강화하고 MMP-13 합성을 억제해 세포 밖 기질 분해를 효과적으로 억제한다.또한 이러한 G Rg1의 효과는 향상된 PI3K/AKT 신호전달에 의해 부분적으로 매개됨을 확인하였다.
또한, GRg1은 염증 매개체의 활성을 억제하고 관절 연골 손상을 감소시킬 수도 있습니다.Cheng 등 [35]은 GRg1의 효과를 관찰하기 위해 인간 연골세포의 in vitro 모델과 쥐 OA의 in vivo 모델을 사용하였다.GRg1이 il-1로 유도된 인체 연골세포 MMP-13, COX-2, PGE2 유전자와 단백질 발현을 억제하고 Col2A1과 ACAN 분해를 막아 연골 변성을 늦추는 것을 발견했다.이는 GRg1이 OA 치료에 잠재적인 임상적 이점이 있음을 시사한다.
진세노사이드 Rg3 3.3
Ginsenoside Rg3 (Ginsenoside Rg3, G Rg3)은 tetraethylene triterpene glycoside 입수 할 수 있는 량의 신진대사 Rb1, Rb2, Rb3, Rc와 Rd. 수산 그룹에 3b, 12b, 그리고 20 pro-S 위치와 β로 변환 할 3-hydroxy 그룹-D-glucopyranosyl-β-D-glucopyranoside dammarane다.프로토파낙사트리올 형태의 진세노사이드 (ginsenoside) [36]이다.
in vitro 연구에서는 인간 OA 연골세포에 대한 G Rg3의 보호효과를 조사하였다.그래서 et al. [37] 자극과 chondrocytes IL-1 β, mmp-1의 증가를 보여주는, MMP-3 그리고 MMP-13 수준 및 COL2A1의 감소와 ACAN 표정을지었다.세포에서 다루어 IL-1 β과 함께 GRg3, mmp-1의 수준과 MMP-13보다 낮았IL-1로 치료 세포 에서만, 그리고 COL2A1의 표현 수준 본 ACAN 낮은 값으로 돌아 갔을 때 세포들이 교양 IL-1 앞에서 β 혼자다.게다가, 조사에 따르면 IL-1 β 자극의 증가로이어 혼자 chondrocytes 리드 senescence-associated β-galactosidase (SA-β-Gal) 긍정적인 세포는 동안의 코 컬 IL-1 β과 GRg3을 크게 억제 한 표식이 노화의 표현이다.또한 GRg3로 배양한 조골세포가 대조구보다 유의적으로 높은 증식 및 텔로머라아제 활성을 보였다.위의 연구는 GRg3가 골관절염에서 연골세포 노화의 영향으로부터 세포를 보호할 수 있음을 보여준다.
또한 GRg3는 sirt1-매개 항세포사멸 및 항염증 기전을 조절함으로써 OA에 효과를 발휘할 수 있다.Ma et al. [38] 사용 종양 괴 자극하는 요인 (TNF)-α TC28a2 인간 chondrocytes을 유도하는 chondrocyte 손상에 의해 그 역전 GRg3 SIRT1의 억압이 표현 발견 TNF-α와 또한 활성화 SIRT1/PGC-1a/SIRT3 경로를 TNF-α을 억제-induced acetylation의 acetylated cyclophilin D (CypD)이다.이로 인해 미토콘드리아 기능부전과 활성산소종 (reactive oxygen species, ROS) 축적이 감소되어 tnf로 유도된 세포사멸이 개선되었다.게다가, 그것은이 발견 되었다는 GRg3 SIRT1의 이치에 역행 활성화/PGC-1a/SIRT3, 중재의 억제 p38 MAPK, 그리고 NF-KB 전위에 따라서 downregulates TNF-α-treated 세포다.요약하면, 아래 TNF-α 자극, GRg3 chondrocytes IL-8의 생산을 줄이고 MMP-9 할 수 있을 통해 SIRT1/PGC-1a/SIRT3/p38 MAPK/NF-KB 신호 경로, 으로써 OA을 치료하는 목적을 달성하다.
진세노사이드 Ro 3.4
Ginsenoside Ro (G Ro) is a type of ginsenoside with a triterpene structure. Some studies have shown that G Ro exerts an anti-inflammatory effect by directly inhibiting the TLR4 signaling pathway, indicating that G Ro can be used as a natural therapeutic compound for inflammation-related diseases [39].
장 et al. [40] 처음 G Ro의 사멸 비율을 억제 할 수 있다고 보고 IL-1 β-induced 쥐 chondrocytes 사멸의 표현이 단백질을 홍보 한다.또한 COX-2, MMP-3, MMP-9과 같은 염증인자의 발현을 억제하여 항염증 효과를 발휘할 수 있다.게다가, 그것은 G Ro의 활성화를 억제 한 다는 것을 발견 NF-KB phospho p65 IL-1에 의해 자극에 β chondrocytes, 그로 나타내 IL-1 억제 β-induced 세포 사멸과 염증 NF-KB 억제 작용을 한다.
기타 진세노사이드 단량체 3.5
현재 OA의 다른 ginsenosides를 이용한 치료에 대한 연구는 상대적으로 적다.그러나 Rb2, Rh, Rc, Rd, Rf를 포함한 ginsenosides 가 MMPs의 발현을 억제하여 항염증 효과를 발휘할 수 있으며, OA의 치료를 위한 잠재적인 약물이 될 가능성이 있다는 연구 결과가 있다.다만 작용 메커니즘에 관련된 대상을 조사하려면 추가적인 연구가 필요하다 [41].Lee 등 [42]은 여러 사포닌을 포함한 ginsenosides Rd, Rf 및 F4가 비세포독성 농도 (1-50 M)에서 IL-1P를 처리한 연골세포에서 MMP-13의 발현을 억제할 수 있음을 발견하였으며, 가장 두드러진 억제제는 ginsenosides F4와 Rg3이다.추가적인 연구를 통해 GF4는 p38 미토겐 활성화 단백질 키나아제의 활성을 강하게 억제하여 MMP-13의 활성을 억제할 수 있음이 밝혀졌다 [43].
게다가, 연구들은 GRb2이과 GRg5에 세포 사멸과 매트릭스를 억제 할 수 있 피해 OA 쥐 관절 chondrocytes, 뿐만 아니라 억제 IL-1 β 그리고 TNF-α, 그렇게 함 으로써 진행을 늦추 거나의 심각성 관절염과 관절 연골 손상을 방지하 는데 [44, 45]다.Zhang 등 (45)은 인대를 절개하고 내측 반월상을 제거하여 골관절염 쥐 모델을 준비한 후, GRg5를 다른 용량의 투여하여 그 효과를 관찰하였다.15 mg Rg5는 OA rat 모델에서 연골변성을 현저히 방지하고 활액붕괴를 방지할 수 있음을 확인하였다.쥐를 GRg5로 처치한 결과 Col2A1, ACAN 및 type II collagen의 발현량을 증가시키고, MMP-13, IL-1P, TNF-a, NO 및 iNOS의 발현량을 감소시켜 GRg5가 OA 쥐에서 연골분해를 방지하고, 활액염증을 억제하며, 연골세포 사멸을 유도할 수 있음을 증명하였으며, 따라서 골관절염의 치료에 사용될 수 있다.
연구에 따르면ginsenoside Rcp-catenin과 Runx2의 고전적 Wnt 경로를 활성화함으로써 조골세포 분화와 기질화 (matrix mineralization)를 촉진하고, 골표지자의 발현을 상향조절하여 골형성을 증가시킬 수 있다 [43].
다수의 ginsenoside 와의 시너지 처리 3.6
OA를 치료하기 위해 다양한 ginsenoside를 복합적으로 사용하는 것도 현재 연구 방향 중 하나이다.일부 학자들은 ginsenoside Rd와 ginsenoside Re로 구성된 화합물 ginsenoside를 활성 성분으로 준비하여 OA의 치료를 위한 약물로 사용하기도 한다 [46].Siddiqi 등 [47]은 신선한 인삼 뿌리로부터 Rg5:Rk1 혼합물을 찌고 건조하기를 반복하여 분리하였으며, 마우스 MC3T3-E1세포의 성장과 분화에 미치는 영향을 연구하였다.Rg5:Rk1은 MC3T3-E1세포의 성장을 용량 의존적으로 자극하고, 콜라겐 합성을 상향 조절하며, 골기질 발달에 증식 및 합성 효과가 있음을 확인하였다.또한 in vitro에서 MC3T3-E1세포의 분화와 광화작용을 유도하였다.Rg5:Rk1이 MC3T3-E1세포의 성장과 분화에 미치는 영향은 BMP-2/Runx2 신호전달 경로의 발현과 밀접한 관련이 있다.Rg5:Rk1은 골세포 분화 촉진 및 적절한 골 형성에 유용할 수 있으며, OA 치료를 위한 잠재적인 약물이 될 수 있다.
또한, 연구에 따르면 다양한 ginsenosides를 함유 한 전통 한약 화합물 또한 OA의 치료에 일정한 전망이 있습니다.Qinqi Rheu-matism Formula (QRF)는 류마티스 관절염 치료를위한 임상 경험 Formula입니다.Pseudostellariae (Kouziqi), Radix Gentianae Macrophyllae (Qinqiao), Fructus Corni (Shanzhuyu)로 구성되어 있다.수지 등 [48]은 오아에게도 일정한 치료효과가 있다고 추측했다.네트워크 약리학 방법을 사용하고 체계적인 네트워크 데이터베이스를 기반으로 OA 개입을 위한 QRF 대상 네트워크를 구축하였다.단의 기동대의 적극적인 행동의 재료와 메커니즘 분석도 OA이 예측 되었고, 그리고 그것은에 단의 기동대이 행동 할 지도 모 른 다는 결론었IL-6 같은 목표, TNF과 IL-1 β 같은 유효 성분을 통해 G 회신, G Rb1 GRg1 그리고 GRd, IL-17 신호를 규제하는 경로, TNF 신호 경로, Th 17, 차별화 Toll-like 수용체 신호 경로, 그리고 osteoclast 차별화 신호 경로, 등 OA에 대한 개입을 달성 하기 위해,OA에서 QRF 중재에 대한 임상연구에 참고자료를 제공하고 있습니다.Huoxue 주유 캡슐은 Angelica sinensis, Panax noto삼, Boswellia serrata, borneol, Rhizoma Corydalis 및 Astragalus membranaceus를 20:10:4:4:6:1 비율로 구성 한 전통 한약 제조법입니다.주요 활성 성분은 G Rg1과 G Rb1 등이 있다 [2].Jua et al. [2]은 Huoxue 주유 캡슐이 MIA에 의해 유도된 쥐 OA 모델에서 OA의 발달을 향상시킬 수 있음을 발견했다.
4 요약 및 전망
인삼은 중국의 전통 약재로서 임상 응용 전망이 넓다.진세노사이드의 약리학적 효과에 대한 연구는 주로 항암, 항산화, 면역자극 활성 등에 초점이 맞춰져 있다.그러나 많은 연구에서 진세노사이드가 항염증 효과를 통해 OA를 비롯한 다양한 염증성 질환을 예방하고 치료할 수 있다는 증거가 제시되고 있다.
OA는 노인에게 주로 발병하는 질병으로서 연구자들의 관심이 높아지고 있다.현재 연구에 따르면 ginsenosides는 OA에 여러 경로를 통해 치료 효과를 발휘할 수 있습니다.Ginsenosides는 조골세포 사멸에서 주요 인자인 Bax/Bcl-2의 발현비를 조절하거나, 조골세포 사멸을 억제하거나, 조골세포 증식을 촉진하여 조골세포를 보호할 수 있다.그러나 이와 관련된 조절신호 경로는 아직 명확하지 않아 추가적인 연구가 필요하다.둘째, ginsenosides는 NF-KB, Notch 및 p38 MAPK와 같은 신호경로를 통해 OA 세포에서 염증신호인자의 발현을 억제하여 항염증 효과를 발휘할 수 있다.또한 ginsenosides는 연골세포 노화를 억제하여 OA 연골 손상의 진행을 막을 수 있습니다.진세노사이드는 항염증 효과 외에도 어느 정도의 항산화 스트레스 [49]도 있다.또한 항산화 스트레스는 OA를 치료하는데 실행 가능한 방법이지만 [50], 항산화 스트레스 측면에서 ginsenosides 가 OA에 영향을 미치는지에 대한 연구는 거의 없었으며, 구체적인 기전은 아직 더 많은 연구가 필요하다.
In summary, with the deepening of research on ginsenosides, ginsenosides and their metabolites and derivatives can be used as effective drugs for the prevention and treatment of OA. Further research is needed on their therapeutic mechanisms to help develop OA treatment drugs and the clinical application of ginsenosides.
참조:
류마티스성 질환에 대한 인삼과 진세노사이드의 개선효과 (YI Y S.인삼연구지 2019, 43(3):335-341.
[2] JUA L J, HUA P P, CHEN P, 그 외.Huoxuezhitong 캡슐은 통해 mia로 유발된 쥐의 골관절염을 개선합니다 sup-PI3K/Akt/NF-B 경로 [J]를 누른다.Biomedicine &Phar-macotherapy, 2020, 129:110471-110482.
[3] 두안차오, 저우시앙, 천옌 외.토끼 무릎 골관절염에서 ginsenoside Rgl이 연골세포의 세포사멸에 미치는 영향 (J.중국의학지, 2018년,33(12):2387-2392.[4] 왕동수, 우신민, 임동매 외.진세노사이드 (ginsenosides)의 위암 억제 효과에 대한 연구 진행.전문연구, 2022, 44(3):118-123+128.
리취안, 차이이후이, 가오지에 등 [5].인삼의 현대 약리학적 효과에 대한 연구 진행.귀양한의학지 2019년, 41(5):89-92.
[6] 바오리샤, 왕후팡, 양진잉 등.ginsenosides 가 쥐의 골관절염에 미치는 영향 (J.저장 임상 의학, 2021, 23(1):4-7.
[7] JI H K, YOUNG S Y, MI Y K 등.ofpanar 인삼의 주요 활성 성분인 ginsenosides의 역할, 염증성 재-sponses 및 질병에서 [J].인삼연구지 2017, 41(4):435-443.
[8] 가오젠, Lv 샤오와.인삼의 화학성분 및 약리학적 효과에 대한 연구 진행.한의학헤럴드, 2021, 27(1):127-130+137.
[9] AHMED T, RAZA S H, MARYAM A 등.신경보호제로서의 Ginsenoside Rb1:고찰 [J.뇌연구 불-에틴, 2016, 125:30-43.
[10] 모하난 P, 수브라마니얌 S, 마티얄라간 R 외.ginsenosides Rb 1, Rg1 및 Rg3의 분자 신호 및 그들의 작용 방식 [J]. 인삼학회지 재검색, 2018, 42(2):123-132.
[11] O'BRIEN M S, MCDOUGALL J. Age and frailty as the risk factors for the 발병의 골관절염 [J].「 mechanism ofAgeing and Development 」, 2019, 180:21-28.
[12] LINN S, MURTAUGH B, CASEY E. 골관절염 발생에 있어서 성호르몬의 역할 [J.PM&R, 2012, 4(5):S169-S173.
[13] 프란시스코 V, 페레즈 T, 피노 J 등이 있다.생체역학, ob 성, 그리고 골관절염.아디포카인의 역할:제방이 무너질 때 [J. Journal of Orthopaedic Research, 2018, 『 한국행정학보 』 36 (2):594-604.
[14] 알리자이 H, 뢰머 F W, 하야시 D 외.MRI-based semiquantitative grading method를 이용하여 평가된 무릎 골관절염의 연골손실 위험인자에 대한 업데이트.유로-피안방사선학, 2015, 25(3):883-893.
[15] 프란시스코 V, 페레즈 T, 피노 J 등이 있다.생체역학, ob 성, 그리고 골관절염.아디포카인의 역할:제방이 무너질 때 [J.Journal ofOrthopaedic Research, 2018, 36(2):594-604.
[16] 정 L, 장 Z J, 현 P 외.조골세포 기능장애와 osteoarthr-itis의 진행에 있어서 metab-olism의 역할 (J.고령화 연구 검토, 2021, 66:101249-101266.
[17] ZHAI G J, 골관절염 [J]의 대사 경로 변경.대사산물, 2019, 9(1):11-22.
[18] 왕 H, 왕 Q, 양엠 외.골관절염의 진행 중 조직형성 및 선천적 면역:활액낭염이 연골분해에 영향을 미치는가.세포생리학회지, 2018, 233(2):1342-1358.
[19] SKOU S T, ROOS E M, 무릎과 고관절 골관절염 환자를 위한 물리치료: 감독, 적극적인 치료는 현재의 최선의 방법이다.Clinical and Experimental Rheumat-ology, 2019, 37(120):0112-0117.
[20] 양 X,린 XJ.골관절염 치료 연구 진행 [J.Chinese Journal of Orthopaedics and Traumatology, 2019, 34(9):900-903.
[21] HERMANN W, LAMBOVA S, MULLER-LADNER U, 골관절염의 현재 치료 옵션 [J.류마트 (Current Rheumat)-ology Reviews, 2018, 14:108-116.
[22] 주은, 호우제이, 마 그 외.네트워크 약리학 identif-골관절염 치료에서 shaoyao gancao decoction의 작용 기전을 [J.Medical Science Monitor, 2019, 14(25):6051-6073.
[23] 컬리포드 D J, 마스켈 J, KIRAN 한, et al.The life-time risk of total hip and knee arthroplasty:results from The UK general practice research database [J] (영어).골관절염과 연골, 2012, 20:519-524.
[24] HOU PW, FUP K, HSU H C 등.전통적인 중국 medi-cine 입원 환자 무릎 골관절염 [J.Journal ofTra-ditional and complementmedicine, 2015, 5(4):182-196.
[25] 주 Q G,리 J H, 팡 M 등이 있다.중국식 마사지 (Tui Na) 가 무릎 골관절염 환자의 등속성 근력에 미치는 영향.ofTraditional Chinese Medicine, 2016, 36(3):314-320.
[26] 윙 S S, 와이트 S, 원 C 등.중국어 (Chinese)의 한자어 (漢字語)에 관한 연구 herbal medicine DAEP 덜어 the osteoarthritic knee pain in rats[J.한의학, 2019, 14:55.
[27] 팬 B, 조우가, 팡 F 등.국내외 골관절염의 연구 현황 및 치료 진행 현황 [J.대한한의학회지 (korean Journal of Basic Medicine in Traditional Chinese Medicine) 2019, 27(5):861-865.
[28] 청 W D, 우 D Y, 주오 Q 등.Ginsenoside Rb1 pre-vents interleukin-1 beta 가 사람 관절연골세포에서 염증과 세포사멸을 유도하였다 [J].International Orthopaed-ics, 2013, 37(10):2065-2070.
[29] 아라빈탄 A, 호사인 M A, 김 B 외.ginseno-side Rb 1은 연골 분해 예방을 통해 폐경 후 쥐에서 monoiodoacetate로 유발된 골관절염을 억제한다 [J].인삼연구지 2021, 45(2):287-294.
[30] Gao Z. 약용식물인 인삼의 활성성분 ginsenoside Rb1이 전방십자인대 절제를 한 쥐에서 골관절염 염증과 단백다당체 분해에 미치는 영향 (J.Molecular Plant Breeding, 2022, 20(14):4800-4806.
[31] Wang W. Experimental study on the regulation of matrix metalloproteinase-13 by ginsenoside Rb1 through the Notch signaling pathway through the osteoarthritis (골관절염 예방을 위한 진세노사이드 Rb1의 조절에 관한 연구) [D].충칭:충칭의과대학, 2015.
[32] 호사인 M A, 알람 M J, 김 B 외.Ginsenoside-Rb1은 rabbit[J]에서 down-regulation ofp-Akt, p-P38, p-P65 신호전달을 통해 골연골 파괴를 방지한다.phytomedi-신, 2022, 100:154039.
[33] 황유민.쥐 골관절염에 대한 ginsenoside Rg1의 치료효과 및 관련기전 [D].난징:난징의과대학, 2015.
[34] 황임, 우디, 팬 WM.[J] PI3K/Akt signaling을 통한 il-1b 유도 미토콘드리아-activ-ated 사멸로부터 조골세포의 보호 (Protection ofginsenoside Rg1 on chondrocyte from IL-1b-induced mitochondria-activ-ated apoptosis through PI3K/Akt signaling) [J.분자 및 세포 생화학, 2014, 392(1):249-257.
[35] 청 W D, 징 J H, 왕 Z 외.Chondroprotective 효과 of ginsenoside Rg 1 in human osteoarthritis chond-rocytes and a rat model of anterior cruciate ligament transec-tion[J] (원저).한국영양학회, 2017, 9(3):263-275.
[36] WON H J, KIM H I, PARK T, 외.비임상약제-ginsenosides의 운동거동 (J.인삼재연구지, 2019, 43(3):354-360.
[37] 그래서 M W, LEE E J, LEE H S, et al.인간 osteoarthritic chondrocytes에 대한 ofginse-noside Rg3의 보호 효과 [J].현대류마티스학, 2012, 23(1):104-111.
[38] 마 CH, 추 W C, 우 CH 등.Ginsenoside Rg3 At-테누에이트 TNF-a-Induced 손상 in chondrocytes sirt1-매개 항세포자멸사 및 항염증-토리 기전 조절을 통하여 [J.산화방지제, 2021, 10(12):1972-1986.
[39] XU H L, CHEN G H, WU Y T 등이 있다.pamnr 인삼의 oll-anolic saponin인 Ginsenoside Ro는 receptor 4 signaling pathway와 같은 toll을 직접 억제함으로써 항염증 ef-fect를 발휘한다 [J].인삼연구지, 2022, 46:156-166.
[40] 장 X H, t. Ginsenoside Ro 억제 XU X X, XU에-terleukin-1 β-induced apoptosis and inflammation in NF-KB를 억제함으로써 쥐의 조골세포 [J]다. Chinese Journal of Natural medicine, 2015, 13(4):283-289.
[41] LEE S Y, ginsenosides에 의한 matrix metalloproteinase 저해의 항전이 및 항염증 효과 (J.바이오-의약품, 2021, 9(2):198-218.
[42] LEE J H, LIM H, SHEHZAD O, 외.ko-rean 홍삼의 Ginsenosides는 관절 연골세포에서 matrix metalloproteinase-13발현을 억제하고 연골 분해를 방지합니다 [J].유럽약리학회지 2014, 724(1):145-151.
[43] 양엔, 장 X,리 L F 등.Ginsenoside rc는 생체 내에서 난소로 유발된 골다공증에서 골 형성과 체외에서 골원성 분화를 촉진한다 [J].International jour-nal ofMolecular Sciences, 2022, 23(11):6187-6209.
[44]리 L,리 X,시 Y 등.산화스트레스로부터 관절연골세포를 보호하는 ginsenoside Rb2의 기전에 대한 연구 (J.Chinese Journal of Orthopaedics, 2018, 26(9):845-849.
[45] 장 P. 진세노사이드-rg5 치료는 골관절염의 rat 모델에서 연골세포의 사멸과 연골기질의 분해를 억제한다 [J].종양학 보고서 (Oncology Reports), 2017, 37(3):1497-1502.
[46] KIM Y O, LEE S W, KIM D H, 외.류마-토이드 또는 퇴행성 골 질환과 같은 골 질환을 예방 또는 치료하기위한 의약품 콤포-션, ofginsenoside Rd 및 ginsenoside Re로 구성된 복합 진세노사이드를 활성 성분으로 구성:KR1856477-B1[P].2018-05-14다.
[47] 시디키, 시디키 MZ, 안 S 등.ginsenosides Rg5:Rk1의 자극효과 murine osteoblastic MC3T3-E1세포에 [J.Phytotherapy Research, 2014, 28:1447-1455.
[48] Su J, Zhou R, Wang M 외.네트워크 약리학을 기반으로 한 골관절염에서 Qinci 류머티즘 포식의 활성 성분 및 작용 기전 예측 (Prediction of active ingredients and mechanisms of action of Qinci rheumatism formula intervention in osteoarthritis)현대한의학회지 2022, 24(3):476-487.
[49] 행케.산화적 스트레스의 Rg1억제에 의한 호르몬 유발 대퇴골두 괴사 예방에 관한 실험적 연구 [D].난징:난징의과대학, 2018.
[50] 하간청, 저우판구.산화 스트레스 반응과 골관절염과의 상관관계 및 항산화 스트레스 약제의 적용에 대한 연구 진행.대한난치병학회지, 2021, 20 (1):94-98.


 영어
영어 프랑스
프랑스 스페인
스페인 러시아
러시아 한국
한국 일본
일본




