Natural Xanthohumol in Hops Extract Enhances Bone Health Product Upgrades
Withthe growing emphasis on healthy living, modern consumers are increasingly prioritizing bone nutrition and daily care다. Among numerous natural plant-derived active ingredients, xanthohumol—a compound sourced from hops—has emerged as a focal point, garnering significant attention from both research and industry sectors.
Xanthohumol is a unique natural flavonoid compound found exclusively in hops. It possesses excellent antioxidant properties and demonstrates promising potential in maintaining cellular health. Research indicates this compound helps support osteoblast activity while regulating osteoclast activity, offering new avenues for developing bone-related dietary supplements and functional foods. Currently, multiple international patents have been secured for xanthohumol applications, indicating broad industrialization prospects.
Adhering to the philosophy 의“Natural Science, Healthy Future,” Green Spring Technology now introduces high-purity, premium-quality xanthohumol powder extracted from hops. We are committed to providing stable, reliable natural ingredient solutions for global clients, empowering brands to develop more innovative and market-competitive bone nutrition products, and jointly advancing the health industry's upgrade.
1 Green Spring Technology High-Purity Xanthohumol: Multi-Pathway Regulation of Bone Metabolism and Cell Differentiation—An Innovative Raw Material Solution Backed by In Vitro Evidence
Xanthohumol, a flavonoid compound derived from hops, demonstrates distinct in vitro activity in regulating bone metabolism. Its multi-target mechanism influences osteoblast and osteoclast differentiation processes, demonstrating development potential as a functional bone nutrition ingredient.
At the molecular level, xanthohumol significantly upregulates Runx2 expression and promotes differentiation markers (e.g., ALP, osteocalcin) in osteoblasts. Simultaneously, it inhibits adipogenesis by suppressing the PPARγ signaling pathway, thereby promoting mesenchymal stem cell differentiation toward osteogenic differentiation. Regarding antioxidant effects, anthohumol activates the Nrf2-ARE pathway to enhance intracellular antioxidant enzyme expression (e.g., HO-1, NQO1), mitigating oxidative stress impacts on osteoblast activity.
In osteoclast regulation, anthohumol inhibits RANKL-induced NF-κB activation by reducing IκBα degradation and p65 nuclear translocation. Simultaneously, it inhibits Ca²⁺ oscillations and the NFATc1 signaling pathway, downregulating key osteoclast differentiation markers (e.g., TRAP, CTSK). MAPK pathway studies indicate that anthoxymol suppresses ERK, p38, and JNK phosphorylation, thereby affecting c-Fos and NFATc1 transcriptional activity.
Green Spring Technology employs proprietary extraction processes to provide epigallocatechin gallate (EGCG) raw material with >98% purity, featuring distinct HPLC fingerprint profiles and batch consistency. This material exhibits excellent stability in both aqueous and lipid-soluble systems, making it suitable for developing various dosage forms such as solid beverages and soft capsules. We provide comprehensive in vitro cellular experimental data support, including osteoblast differentiation assays, osteoclast formation inhibition studies, and antioxidant activity measurements, serving as a reference for product development.
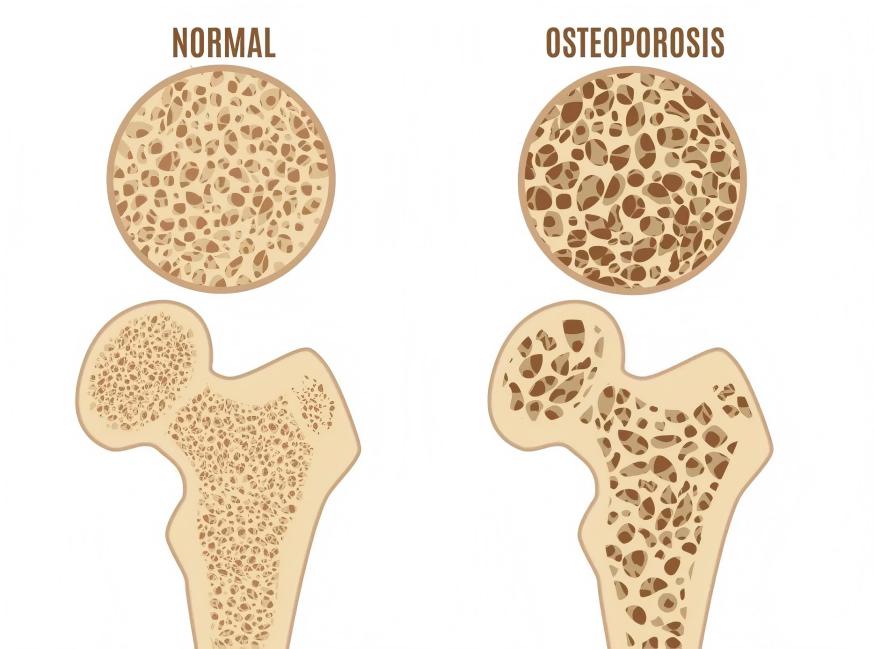
2 Green Spring Technology Xanthohumol: Multi-Pathway Regulation of Cellular Function, Empowering Next-Generation Bone Nutrition Innovation
Xanthohumol, a natural bioactive compound derived from hops, has garnered significant attention in the field of bone nutrition in recent years. Its multi-targeted properties in cellular signaling and metabolic regulation offer new avenues for developing innovative bone nutrition products.
Research indicates that xanthohumol interacts with multiple cellular signaling pathways to maintain the healthy equilibrium of bone tissue. By influencing RANKL-mediated cellular signaling, it participates in regulating various cellular functional pathways including NF-κB, Ca²⁺/NFATc1, and MAPK, thereby supporting bone health at the molecular level.
At the mechanistic level, p-Cresol has been found to regulate IκB protein metabolism, influencing NF-κB's intracellular localization. Simultaneously, it modulates Ca²⁺ signaling frequency, positively affecting NFATc1 activity. Furthermore, p-Cresol exhibits regulatory effects on EPK1/2 and c-fos expression within the MAPK pathway. These multifaceted mechanisms provide a scientific rationale for p-coumaric acid's application in bone nutrition.
Green Spring Technology employs innovative extraction processes to produce high-purity, highly stable p-coumaric acid raw materials. Our products exhibit excellent biocompatibility and compatibility, making them suitable for dietary supplements, functional foods, and specialized dietary products. We are committed to providing partners with premium natural raw material solutions, jointly advancing the development of bone nutrition products toward greater efficiency and innovation.
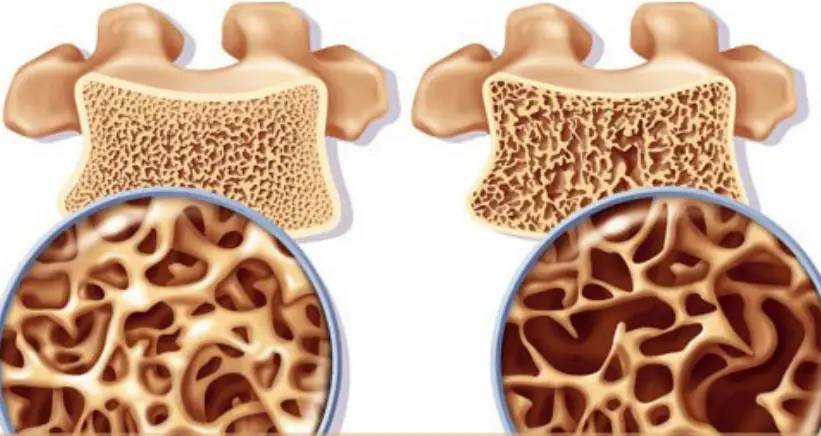
3 Innovative Bone Nutrition Solutions: Green Spring Technology's High-Purity Xanthohumol Powder, Empowering Product Upgrades
As modern society increasingly prioritizes healthy aging, the bone nutrition sector faces renewed demand for product innovation. Xanthohumol—a bioactive flavonoid from hops—has demonstrated multi-pathway potential in regulating bone metabolism through extensive cellular studies, opening new avenues for advanced bone health products.
Green Spring Technology leverages advanced extraction and purification techniques to introduce high-purity, high-stability xanthohumol powder with the following core advantages:
✨ Purity >98%, backed by complete HPLC detection spectra and a rigorous quality control system ensuring batch-to-batch consistency;
✨ Excellent bioavailability and compatibility, suitable for diverse formulations including solid beverages, soft capsules, and tablets;
✨ Comprehensive in vitro cellular experimental data support, including multi-dimensional research outcomes on osteogenic differentiation, antioxidant activity, and cellular metabolism.
Learn More About Our One-Stop Solution for Standardized Hop Extract Ingredient.
We are committed to providing partners with scientifically validated, commercially valuable raw material solutions that help clients:
· Break through the homogenized competition of traditional bone nutrition products by creating innovative offerings with differentiated competitive advantages;
· Gain end-to-end technical support spanning ingredient mechanism research to product development;
· Accelerate product R&D cycles to swiftly respond to market demands.
Green Spring Technology collaborates with industry partners to leverage natural science and technology, jointly advancing the professionalization and scientific upgrading of bone health products. We deliver more effective and safer nutritional solutions for consumers.
Contact us at helen@greenspringbio.com or WhatsApp: +86 13649243917 for complimentary samples and technical documentation.
참조
[1] 쑤리징 (Xu Lijing), 첸밍현 (Chen Mingsheng), 시레이 (Si Lei).골다공증의 건강경제학적 평가 현황, 과제 및 유의사항에 대한 자료입니다.2021년 Chinese Journal of Endocrinology and Metabolism,
[2] 왕은 Wenhui다.골다공증 치료제의 효과와 발전.대한내과학회지 2021, 56(11):1189-1192.
[3] 린 Canbin다.골다공증 치료에 다른 유형의 비스포스포네이트 약물의 임상적 효능.이성약물사용학회지 2021, 14(32):109-111.
[4] 위안춘옌 (Yuan Chunyan), 렌뮤리안 (Ren Mulian)폐경 후 골다공증에 대한 성호르몬 치료.산부인과학회지, 2020, 36(7):494-497.
[5] 구항수애 (Qu Hangshuai), 정정민아 (Zheng Jingmin)식물 플라보노이드의 골다공증 방지 효과에 대한 연구 진행.중국골다공증학회지 2021, 27(10):1529-1533.
[6] Liu Xiaoyan, Xia Tian Shuang, Dong Zhiming, 외.골다공증 치료에서 홉의 적용과 전망.약학실무학회지 2020, 38(6):492-495.
[7] Aggarwal D, Upadhyay SK, 싱 R,et al.에 대한 최근 특허 치료 활동 of xanthohumol: 호프의 prenylated chalconoid (Humulus lupulus L.) [J]다. Pharm Pat Anal,2021,10(1):37-49.
[8] 오카모토 K, 나카시마 T, 시노하라 M, 외 Osteoimmunol- ogy:면역계와 골격계를 통합하는 개념적 틀 [J].Physiol Rev, 2017년 97 (4):1295-1349.
[9] 무루가난단 S, 이오네스쿠 AM, 시날 CJ.교차로에서 지방세포 및 골세포 분화 프로그램의: 미래 치료적 관점 (Future Therapeutic Perspectives) [J]다.Int J Mol Sci,2020, 21일 (7):2277다.
-
Prev
Natural Hop Extracts Empower Innovation in Bone Health Products
-
다음
Natural Hop Extract Fuels Innovation in Wellness Product Formulations


 영어
영어 프랑스
프랑스 스페인
스페인 러시아
러시아 한국
한국 일본
일본



