D 알룰로스의 근원은 무엇인가?
국제희귀당학회 (ISRS)는 희귀당을 자연계에서 드물게 발생하는 단당류 및 그 유도체로 정의한다 [1]다.ISRS 정의에 따르면,D-allulose is considered 한rare sugar as 한diastereoisomer at the C-3 positi에의D-fructose. D-alluloseis a low-calorie sweetener. Taking a 100g/L sucrose solution as 한example, D-allulose is 70% as sweet as sucrose [2], but only 0. 3% 의the energy 의sucrose[3]. At the same time, D-allulose has unique 생리적functions. As an inhibitor 의hepatic lipogenic enzymes 그리고intestinal α-glucosidase[4], D-allulose is hardly metabolized 그리고absorbed 에서the small intestine[5], which can further reduce postprandial hyperglycemia, improve insul에서resistance 그리고reduce the accumulation 의body fat, which is 의great benefit 을both obesity 그리고diabetes [6~7]. In addition, D-allulose has been declared “generally recognized as safe” (GRAS) by the US 음식그리고Drug Administration (FDA) [8] 그리고can be used in food 그리고medicine.
D Allulose is a 새로 운rare monosaccharide that is safe 을health. It has physiological properties such as reducing blood glucose response, reducing liver fat production, maintaining body weight, anti-oxidation 그리고protecting blood vessels. D-Allulose is increasingly valued by researchers 을its special nutritional 그리고biological functions. Since the content 의D-allulose in nature is very low, it is difficult to prepare it by chemical methods. At present, the major 생산method is the enantioselective isomerization between D-fructose and D-allulose[9~10]. 이ketose 3-isomerase involved is a research hotspot, which can be obtained 에서different microorganisms. The most commonly used is the D-allulose 3-isomerase 의Agrobacterium tumefaciens[11~12] .
1 생산 기술의 연구 진행
1. 1 Chemical 합성합성법
처음에는 화학적 방법으로 d-알룰로오스를 합성하였다.Bilik 등 [13]은 산성 수용액에서 몰리브덴 데이트 이온의 촉매 작용으로 d-과당이 d-알룰로스로 전환될 수 있음을 발견하였다.
1997년, 도널드 [14]으로 화학적으로 합성 가 D-allulose 준비 1, 4 절, 5-di-O-isopropylidene-β-D-fructopyranose다.그 외에 d-알로-케톤산도 에탄올과 트리에틸아민 [15]을 끓여서 합성할 수 있다.연구가 심화됨에 따라 화학합성방법은 원가가 높고 조작이 위험하며 공정이 어렵고 정화가 복잡하고 생산량이 적고 환경오염을 일으키기 쉬운 단점이 있으며 제품안전성에 대한 연구가 필요하다.그것은 점차 생물 변환 방법으로 대체되고 있다.
1. 2 Bioconversion 방법
d-알룰로스의 생물 전환은 일본 카가와 대학의 켄 이즈모리 교수가 처음 제안하였다.헥시톨을 중간체로 사용하여 희귀 헥소스간의 생물 변환을 완료하는, 즉, 이즈모링 생물 변환법 [16]을 사용한다.이는 diastereisomerase (히드록시기의 이산화 특이), polyol dehydrogenase (케토오스와 당 알코올 사이의 반응을 촉매), aldopentose isomerase (알도펜토오스 이성화 반응) [17]를 포함한다.그 중 d-알룰로스 3-에피머화 효소 (DPE)는 d-과당 및 d-알룰로스를 전환할 수 있다.
1. 2. 1 d-알룰로스 3-에피머화 효소
D-Allulose 3-epimerase는 D-fructose를 D-Allulose로 전환하는 핵심 효소이며 ketose 3-epimerase계열 효소의 일원이다.1993년 이즈모리 등 [16]은 녹농균 치코리로부터 케토오스 이성질체 분해효소를 처음으로 분리, 정제하였다.그것의 최적 제품은 d-타가토스이기 때문에 d-타가토스 3-에피머erase (DTE)로 명명되었다. DTE)이다.또한 Kim 등 [18]은 Agrobacterium tumefaciensstr. C58에서 32.9%의 전환율로 d-과당을 d-알룰로스로 전환하는 것을 구체적으로 촉매하는 효소를 발견하였다.이름은 d-allulose 3-epimerase.최근 여러 미생물원으로부터 D-allulose 3-epimerases 가 점차 발견되고 있으며 (표 1 참조), 이들의 특성에 대한 연구가 진행되고 있다.
1. 2. D-allulose 3-epimerase의 2 특성
The properties 의D-allulose 3-epimerasevary depending on the microbial source. As can be seen 에서Table 1, the 최적temperature for most D-allulose 3-epimerases is 50-70°C, and the optimum pH is 7.0-8.0. The optimum pH for the D-tagatose 3-epimerase의the Rhodobacteraceae is 9.0, while the optimum pH for the D-allulose 3-epimerase의the genus Doria is isomerase has an optimum pH 의6.0. In addition, the activity 의the enzyme can be effectively increased by the addition of metal ions [27], and the optimum metal ion for D-allulose 3-epimeraseis Mn2+ or Co2+.
(1) D-allulose 3-epimerase에 대한 온도의 효과
d-알룰로스의 산업 생산에 열 안정성은 중요합니다.일반적으로, 설탕 산업의 생산에서, 적합한 고온은 원료의 이용률과 생물 전환 속도를 향상시키고, 용액의 점도를 낮추고, 반응물 및 생성물의 용해도를 높이고, [28] 수율을 더 높일 수 있다.그러나 D-allulose 3-epimerase의 열 안정성이 떨어지고, 반감기가 짧아 [29] 산업 생산에 제한을 받는다.따라서, d-알를로오스 3-epimerase의 열 안정성 향상은 알를로오스의 산업 생산에 필요하다.이 중 무작위 돌연변이 발생법과 합리적 단백질 설계법은 단백질 공학 분야에서 효소의 열적 안정성을 향상시키는 대표적인 방법이다 [30-32].
최 등 (19)은 Agrobacterium tumefaciens 로부터 D-allulose 3-epimerase의 돌연변이 균주 S213C, I33L 및 I33LS213C를 얻기 위하여 error prone polymerase chain reaction (error-prone PCR)과 site-directedmutagenesis를 이용하였다.야생형 D-allulose 3-epimerase에 비해 돌연변이 균주인 S213C, I33L 및 I33LS213C의 효소활성에 대한 최적온도는 각각 2.5 °C, 5 °C 및 7.5 °C 증가하였고 50 °C 에서의 반감기는 3.3, 7.2 및 29 증가하였다.9회, 그리고 겉보기 녹는 온도는 3 증가했습니다.1 ℃, 4.3℃ 및 7.6 ℃이다.그 결과 D-allulose 3-epimerase돌연변이 균주의 열안정성이 현저히 향상되었으며, 그 중 I33LS213C 돌연변이 균주는 D-allulose 생성 가능성이 있는 것으로 나타났다.
한편, Zhang 등 [33]은 대장균subtilis의 D-allulose 3-epimerase의 tyrosine 68과 glycine 109에서 각각 site-directed mutagenesis를 통해 Y68I 돌연변이와 G109P 돌연변이를 얻었다.야생형 D-allulose 3-epimerase에 비해 Y68I 돌연변이가 가장 높은 기질결합친화도와 촉매효율을 보였으며, G109P 돌연변이가 가장 높은 열안정성을 보였다.또한, double-site Y68I/G109P mutant 가 생성되어 좋은 효소특성을 보였으며, 이를 입증한 결과 Michaelis 상수 (Km) 가 17.9% 증가하였고, 촉매효율 (Kcat/Km)이 1.2배 증가하였으며, 반감기가 156분에서 260분까지 55°C에서 증가하였고, 외견상 용융온도는 2.4 °C 증가하였다.이는 Y68I/G109P 돌연변이가 D-allulose의 산업적 생산에 적합함을 나타낸다.
(2) D-allulose 3-epimerase에 대한 pH의 효과
D-allulose 3-epimerase의 최적 pH 값은 7.0-9.0으로 알칼리 범위에 있습니다.그러나 설탕 산업에서의 생산은 산성 조건 하에서 수행되는데, 산성 조건은 부산물의 형성과 갈변 반응을 감소시킬 수 있기 때문이다 [34-35].따라서 d-알룰로스 3-epimerase의 반응 pH는 단당류 산업의 생물 전환 요구에 이상적이지 않습니다.보다 나은 생성물을 얻기 위해서는 유전공학을 통해 효소의 최적 반응 pH를 향상시킬 필요가 있다.
(3) D-allulose 3-epimerase에 대한 금속이온의 효과
금속 이온은 D-allulose 3-epimerase에 일정한 영향을 미친다.표 1에서 알 수 있듯이, Clostridium botulinum의 D-allulose 3-epimerase, Clostridium cellulovorans의 D-allulose 3-epimerase, Clostridium butyricum의 D-allulose 3-epimerase, Doria formosa의 D-allulose 3-epimerase, Clostridium tricornutum의 D-allulose 3-epimerase의 최적 금속이온은 Co2+이다.isomerase's의 최적 금속이온은 Co2+.Agrobacterium tumefaciens의 D-allulose 3-epimerase, Pseudomonas cepacia ST-24의 D-tagatose 3-epimerase, Sphingobium sp.의 D-tagatose 3-epimerase, Streptococcus ruminantium의 D-allulose 3-epimerase의 최적 금속이온은 Mn2+이다.
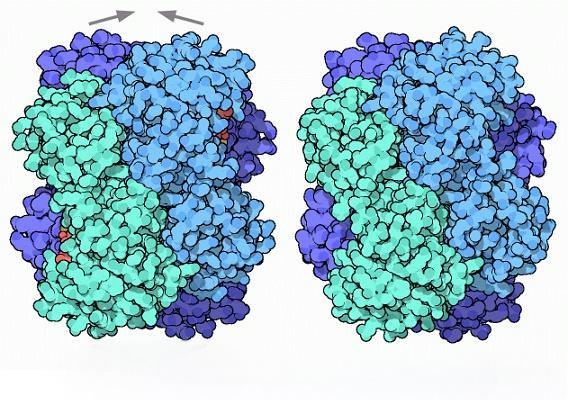
을D-tagatose 3-dehydrogenase 에서Burkholderia cepacia, Itoh et al. [17] showed that the activity does not require the assistance of metal ions, but the addition of metal ions, especially Mn2+, significantly increases the activity. In particular, Clostridium D-allo-hexose 3-epimerase has a strict metal ion dependence, requiring metal ions as cofactors to display activity. In the absence of ions, it is almost inactive, and it shows maximum activity in the presence of Co2+ [36]. In addition, it was found that the cellulase D-allulose 3-epimerase has extremely high thermal stability in the presence of Co2+ [36].
Patel 등 (37)은 n-말단 융합을 위해 효모 상동단백질인 Smt3를 이용하여 Smt3 d-알를로오스-3 이성화효소를 얻고, 최적의 반응조건에서 Smt3 d-알를로오스-3 이성화효소에 대한 이중성 금속이온의 촉매활성을 조사하였다.그 결과 Zn2+, Cu2+, Ni2+의 존재에서는 효소의 활성이 거의 소실됨을 알 수 있었다.Ca2+는 활성에 현저한 저해효과를 나타냈으며 Mg2+, Fe2+ 및 Ba2+는 활성을 변화시키지 않았다.반대로 Mn2+와 Co2+는 검사반응에서 Mn2+의 양 (0.025-0.1 mmol/L)이 매우 낮더라도 효소의 활성을 유의하게 증가시킬 수 있었다.Jia 등 [24]은 Clostridium botulinum D-allo-keto-glucose 3-epimerase에 대한 금속 이온의 영향을 연구하였다.그 결과 EDTA는 D-allo-keto-glucose 3-epimerase의 활성을 완전히 억제하였으며, Zn2+, Mg2+ 및 Cu2+는 효소활성의 일부를 억제하였다.반대로 Co2+와 Mn2+는 효소의 활성을 유의적으로 증가시켰으며, 특히 Co2+는 D-allulose 3-epimerase의 활성을 크게 향상시킬 수 있다.
(4) D-allulose 3-epimerase에 대한 다른 요인의 영향
Except for the D-tagatose 3-epimerase of Pseudomonas citrea ST-24 and the D-tagatose 3-epimerase of Sphingobium sp다.which have D-tagatose and D-fructose as their optimal products, respectively, most of the other allulose 3-epimerases have D-allulose as their optimal product. The equilibrium conversion rate between D-allulose and D-fructose is between 28% and 33% [38].
또한 Kim 등 [39]은 D-allulose 가 borate 와의 높은 착색능력을 가지고 있으며, 이는 D-fructose 가 D-allulose를 추가로 생성하도록 도와준다는 것을 보여주었다.Lim 등 (40)은 보레이트 존재하에서 안정적이고 높게 D-allulose를 생성하기 위해 고정화된 D-allulose 3-epimerase를 원료로 사용하였다.allulose다.주요 메커니즘은 붕산염이 탄수화물과 반응하여 복합체를 형성하고, 복합체가 효소계와 상호작용하여 당의 결합 친화력의 차이를 통해 cis-diol 탄수화물과 관련된 모든 반응의 평형을 변화시켜 [41~42] 높은 전환율을 얻을 수 있다.
2 결론
현재 d-알룰로스를 생산하는데 사용되는 주된 공업용 효소는 d-알룰로스 3-에피머화 효소로, 기질인 d-프럭토스에 대한 친화도와 전환율이 높다.d-알룰로스의 수율을 더욱 높이기 위해 일부 연구자들은 유전공학 기술을 이용하여 전환율이 더 높은 d-알룰로스 3-에피머화 효소를 얻었다.따라서 미생물 숙주에서의 효소 발현 및 분비의 안전성에 대한 연구가 더 진행되어야 잠재적인 식품안전 문제가 발생하지 않을 수 있다.피플 &의 개선으로#39;의 생활 수준 및 건강 인식, 그리고 실험 연구의 심화, d-알룰로스는 더 넓은 발전 가능성을 가질 것이다.
참조:
[1] Zhu Z, Li L, Zhang W 등.D-allulose의 효소 특성 개선 3-epimerase 에서 a thermophilic 유기체 halanaerobium congolense의 을 통해 합리적인 설계다 [J다] 효소와 미생물 기술, 2021, 149:109850.
[2] Ogawa M, Hayakawa S. 희설탕 D-psicose의 식품가공에의 응용 (J.Journal of the Japanese Society for Food Science and Technology-Nippon Shokuhin Kagaku Kogaku kai-shi, 2021, 68(3):101-114.
[3] 볼거 한M, 라스톨 R A, 오루나-콘차 M J 외.D-allulose 가 sucrose와 D-fructose에 비해 컵케익의 물성에 미치는 영향 (J.LWT, 2021년 150조:111989.
[4] Kanasaki A, Niibo M, Iida T. Effect of D-allulose feeding on the hepatic metabolomics 프로 파일 in 남성 wistar 쥐 [J]다. Food 및 기능, 2021, 12(9):3931-3938.
[5] Maeng H J, Yoon J H, Chun K H, etal.D-allulose in의 대사 안정성 biorelevant 미디어 and hepatocytes:비교 과당과 erythritol[J]로.Foods, 2019, 8(10):448.
[6] 하야카와 M, Hira T, 나카무라 M, 외. 분비를 of GLP-1 이지만 GIP 가 강력하게 자극되지 않는 b yluminal D-allulose (D-psi-cose) 쥐에서 [J.Biochemical and Biophysical Research commu-nications, 2018, 496(3):898-903.
[7] 퐁칸 W, 진나옹 K, 프랏차야사쿨 W, 외. d-알룰로스는 비만 유발 인슐린 내성 쥐에서 심장 미토촌-드리아 기능 부전을 약화시키는 심장 보호 효과 b y를 제공한다 [J].유럽영양학회지, 2021, 60(4):2047-2061.
[8] 장 W, 장 T, 장 B 등.효소는 희귀 설탕 생산에 접근 [J].생명공학발전 (Biotechnology Advances), 2017, 35(2):267-274.
[9] Zhao J, Wei H, Chen J, etal.D-allulose in의 효율적인 생합성 Bacillus 항생제 을 통해 D-psicose 3-epimerase 번역 수정 [J.국제생물학회지 (International Journal of Biological) Macromole-cules, 2021, 187:1-8.
[10] 장 J, 루오 W, 왕 Z 등.D-psicose를 위한 새로운 전략과 리 파 아제 공동 사용 a 코 컬 시스템 of engi-neered bacillus subtilis와 escherichia coli와 bioprocess anal-ysis 사용 metabolomics다 [J다] Bioresources and Bioprocessing, 『 한국지방자치학회보 』 2021, 8(1):1-18.
[11] 왕장위, 손장동, 기홍청 외.whole recom-binant Bacillus를 고정화하여 D-fructose 로부터 D-psicose의 높은 produc-tion 항생제 세포 표현하는 D-psicose Agrobacterium에서 3-epimerase tumefaciens다. [J]다.생명공학 and 응용생화학 (적용Biochemistry, 2021):doi:10.1002/BAB.2115다.
[12] 양 P, 주 X, 정 Z 외.의 세포 재생 및 순환 촉매 작용 조작 kluyveromyces marxianus of D-psicose3-epimerase 유전자 에서 agrobacterium tumefaciens for D-allulose 제작 [J.한국미생물생명공학회지 2018년, World Journal of Microbiology and Biotechnology, 34(5):1-7.
[13] 빌릭 5세, 틸라릭 K.당류의 반응은 b y molyb-date를 촉매로 하였다 이온다. 다 lx Epimerization of 케토헥소세스 [J. 화학 Zvesti, 1973, 28:106-109.
[14] 도널드 E J. A new synthesis of D-psicose (d-리보헥술로스) [J.탄수화물 연구, 1997, 5:106-108.
[15] Doner L W. Isomerization of D-fructose by base:liquid chroma-tographic evaluation and the isolation of D-psicose[J].Carbo-hydrate Research, 1979, 70:209-216.
[16] 이즈모리 K, 라흐만 A K, 오카야 H, 에탈.의 새로운 효소인 d-ke-토헥소스 3-epimerase 녹 농 균 sp다. st-24다 [J다] 「 bioscience Biotechnology and Biochemistry 」, 1993, 57(6):1037-1039.
[17] 이토 H, 오카야 H, 칸 R A 외.d-타가토스의 정화와 인격화 3-epimerase 에서 녹 농 균 sp다. st-24 [J.생물과학 Biotechnology and Biochemistry, 1994, 58(12): 2168-2171다.
[18] Kim H J, 이현주 (J, Hyun ju) E K, 김 Y S, 외. 성격 묘사 of D-fructose를 D-psicose로 전환시키는 agrobacterium tumefaciens D-psicose 3-epimerase [J.한국환경미생물학회, Applied and 환경Micro-biology, 2006, 72(2):981-985.
최형기 (Choi J G), 주이 (Ju Y H), 염정아 (Yeom S J)agrobacterium tumefaciens b y random 및 site-directed mutagenesis 로부터 D-psicose 3-epimerase의 thermostabili-ty 개선 [J].정신미생물학 (mental Microbiology), 2011, 77(20):7316-7320.
[20] 양 C, 루안 N, 안 J, 에탈.rhodobacter sphae-roides 가 장내 미생물 및 단쇄지방-ty 산의 조성에 미치는 영향 쥐 [J.저널 음식과 영양연구 (Nutrition Research), 『 한국정치학회보 』 2020, 8(6):288-296.
[21] Zhu Y, Men Y, Bai W, etal.ruminococcus sp.의 escherichia coli에서 D-psicose 3-epi-merase의 과발현 및 그 포텐-tial application in D-psicose 생산 [J].생명공학 Let-ters, 2012, 34(10):1901-1906.
[22] 웨이 H, 장 R, 왕 L, 에탈.로부터 D-psicose 3-epi-merase의 발현 클 로스 bolteae and dorea sp. and bacillus subtilis에서 d-psicose의 전세포 생산 (J.Annals of Micro-biology, 2020, 70(1):1-8.
[23] 장 W, 팡 D, 장 T 등.금속의존형 D-psicose 3-epimerase의 특성 (characteristic of a metal-dependent D-psicose 3-epimerase 에서a novel strain, desmos-pora sp.8437[J.『 한국농식품화학학회지 』, 2013, 61(47):11468-11476.
[24] 지아 M, 무 W, 추 F 외.neu-tral pH를 갖는 D-psicose 3-epimerase optimum from 클 로스 bolteae 대한 D-psicose pro-duction:복제, 표현, 정화, 그리고 특성화 [J.한국미생물학회, Applied Microbiology and Biotechnology, 2014, 98(2):717-725.
[25] Su L, Sun F, Liu Z, etal.bacillus subti-lis에서 clostrid-ium cellulolyticum H10 D-psicose 3-epimerase의 매우 효율적인 생산과 사용 of 이 러한 세포 to 생산 D-psicose다 [J다] 미생물 세포공장, 2018, 17(1):1-10.
[26] 무 W, 장 W, 팡 D, 에탈.clostridium sp 로부터 D-psicose 생성 효소인 D-psicose 3-epimerase의 특성. [J]다.Biotechnology Letters, 2013, 35(9):1481-1486.
[27] Yoshihara A, 코자카이 T, 신타니 T, 외. 정화 그리고 성격 묘사 of D-allulose 3-epimerase 파생 된 from ar-throbacter globiformis M30, GRAS 계 미생물 [J.jour-nal of Bioscience and Bioengineering, 2017, 123(2):170-176.
[29] 장 S, 샤오 W, 주 X, 에탈.D-allulose에 대한 고찰:in vivo me-tabolism, 촉매 메커니즘, 공학적 변형 구성, 바이오생산기술 [J.국경 in 생명공학 그리고 생명공학, 2020, 8:26.
[30] 주즈, 가오 D,리 C, 에탈.Redesign of a novel D-allulose 3-epi-merase from staphylococcus aureus for thermostability and effi-cient biocatalytic.-황색포도상구균으로부터 새로운 D-allulose 3-epi-merase의 재설계 (Redesign of a novel D-allulose 3-epi-merase from staphylococcus aureus production of D-allulose다 [J다] 미생물이 세포공장, 2019, 18(1):1-10.
[31] 첸 Q, 샤오이, 장 W 등.식품산업에서의 전산 단백질 제조에 관한 연구 (Current methods and applica-tions in computational proteindesignforfoodindustry[J])Crit-ical Reviews in Food Science and Nutrition, 2020, 60(19):3259-3270.
[32] 마오 S, 청 X, 주즈 등.D-allulose의 thermostable ver-sion을 공학 3-epimerase from rhodopirellula baltica site-directed mutagenesis를 통해 기초 on B-factors [J] 분석 합니다. 엔-자임과 미생물 기술, 2020, 132:109441.
[33] 장 W, 지아 M, 유 S, 에탈.clostridi-um 으로부터 D-psicose 3-epimerase의 열안정성 및 촉매효율 향상 bolteae ATCC BAA-613 사용 site-directed 돌연변이 발생 [J.한국농식품화학학회지, 2016, 64(17): 3386-3393다.
[34] 장 W,리 H, 장 T, 에탈.dorea sp. cag317으로부터 D-psicose 3-epimerase를 산성 pH 최적치와 높은 특이활성을 갖는 특성 [J.저널 of 분자 촉매 B:효소, 2015, 120:68-74.
[35] Chen J, Chen D, Ke M 등이 있다.재조합 D-allulose 3-epimerase의 특성 from thermoclostridium caenicola D-allulose 생산에 적용 가능성이 있는 [J].분자 bi-otechnology, 2021, 63(6):534-543.
[36] Mu W, Chu F, Xing Q, etal.복제에 대한 수정, 표현, 및 clostridium-cellulolyticum 으로부터 D-psicose 3-epimerase의 특성 H10다 [J다]저널 of 농업 and 식품화학, 2013, 61(43):10408.
[37] 파텔 S N, 샤르마 M, 라타 K 외.D-psicose 3-epimerase b y a novel의 개선된 operational star-bility 단백질 공학 전략, 그리고 과일과 채소로부터 D-psicose 생산 res-idues[J].바이오원천기술, 2016, 216:121-127.
[38] 첸 X, 왕 W, 슈 J 등.D-glucose b y 로부터 D-psicose의 생산 co-expression of D-psicose 3-epimerase and 자일로스 이성질체 [J]. 효소 and 미생물이 기술, 2017, 105: 18-23다.
[39] Kim N H, Kim H J, Kang D I, etal.D-fruc-tose의 전환 이동 을 D-psicose for enzyme-catalyzed epimerization b y 의 addi-tion 붕산 염다 [J다] Applied and Environmental 미생물학, 2008, 74(10):3008-3013.
[40] Lim B C, Kim H J, Oh D K.보-율 [J]의 존재에서 D-psicose의 생산을 위한 안정적인 고정화 D-psicose 3-epimerase.공정생화학, 2009, 44(8):822-828.
[41] Song Y, Nguyen Q A, Wi S G 외.연구논문:십자화과로부터 부가가치 생산물로서 바이오에탄올과 D-psicose의 이중 produc-tion 전략 (Strategy for dual produc-tion of bioethanol and D-psicose as added products from cruciferous 야채 잔류 [J. 구라 기술, 2017, 223:34-39.
[42] 시아 Y, 청 Q, 무 W, 에탈.D-allulose의 연구 진보: an 개요 of physiological 기능, 효소제 바이오트랜스포 (biotransfor)-화장 기술 (mation technologies), 그리고 생산 공정 [J.식품, 2021년, 10 (9):2186다.


 영어
영어 프랑스
프랑스 스페인
스페인 러시아
러시아 한국
한국 일본
일본




